Research Abstract
CRISPR/Cas9ゲノム編集によるレポーター/ドライバー遺伝子をノックインしたトランスジェニックゼブラフィッシュの高効率作製
Efficient generation of knock-in transgenic zebrafish carrying reporter/driver genes by CRISPR/Cas9-mediated genome engineering
2014年10月8日 Scientific Reports 4 : 6545 doi: 10.1038/srep06545
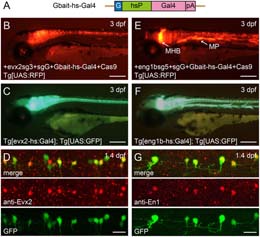
細菌のII型CRISPR/Cas9系は、その簡便性、融通性および効率の高さから、ゲノム編集において急速に利用が拡大している。最近、ゼブラフィッシュにおいて、CRISPR/Cas9系を用いた、相同組換え非依存的なDNA修復による長鎖DNA断片の標的ノックインが達成された。このことから、CRISPR/Cas9を用いてノックイントランスジェニックゼブラフィッシュを効率的に作製できる可能性が浮上した。しかし、この方法を、内在遺伝子座への外来遺伝子の標的挿入にどの程度の効率で用いることができるのかは分かっていない。本論文では、細胞種特異的にGal4あるいはレポーター遺伝子を発現する、ノックイントランスジェニックゼブラフィッシュの効率的な作製を報告する。ゲノム切断を標的とする短鎖ガイドRNA(sgRNA)、ドナープラスミドの切断を標的とするsgRNAおよびCas9 mRNAを、熱ショックプロモーターを含むドナープラスミドと共に受精卵に注入した。我々は、25%を超える頻度で4つの遺伝子座にいくつかの異なるコンストラクトをノックインしたトランスジェニックフィッシュを確立することに成功した。CRISPR/Cas9によるノックインは、簡便性、設計融通性および効率の高さから、トランスジェニックゼブラフィッシュ作製の標準的な手法の1つになると、我々は提案する。
木村 有希子1, 久野 悠2, 川原 敦雄2,3 & 東島 眞一1
- 岡崎統合バイオサイエンスセンター 自然科学研究機構 生理学研究所
- 理化学研究所 生命システム研究センター 循環器分子動態研究ユニット
- 山梨大学大学院 医学工学総合研究部 発生生物学
The type II bacterial CRISPR/Cas9 system is rapidly becoming popular for genome-engineering due to its simplicity, flexibility, and high efficiency. Recently, targeted knock-in of a long DNA fragment via homology-independent DNA repair has been achieved in zebrafish using CRISPR/Cas9 system. This raised the possibility that knock-in transgenic zebrafish could be efficiently generated using CRISPR/Cas9. However, how widely this method can be applied for the targeting integration of foreign genes into endogenous genomic loci is unclear. Here, we report efficient generation of knock-in transgenic zebrafish that have cell-type specific Gal4 or reporter gene expression. A donor plasmid containing a heat-shock promoter was co-injected with a short guide RNA (sgRNA) targeted for genome digestion, a sgRNA targeted for donor plasmid digestion, and Cas9 mRNA. We have succeeded in establishing stable knock-in transgenic fish with several different constructs for 4 genetic loci at a frequency being exceeding 25%. Due to its simplicity, design flexibility, and high efficiency, we propose that CRISPR/Cas9-mediated knock-in will become a standard method for the generation transgenic zebrafish.

