Research Abstract
ヌクレオポリンTprによるオートファジーの制御
Regulation of autophagy by nucleoporin Tpr
2012年11月20日 Scientific Reports 2 : 878 doi: 10.1038/srep00878
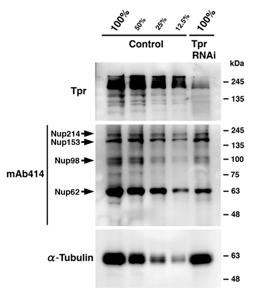
核膜孔複合体(NPC)は、ヌクレオポリンと呼ばれる30種に及ぶ異なるタンパク質群から構成され、細胞質と核との間の物質交換のための出入口として機能する。Tpr(translocated promoter region)はNPCの構成因子であり、核内フィラメントに局在すると考えられている。本研究では、Tprのノックダウンが核膜孔の数を大幅に減少させることを示す。さらに、電子顕微鏡解析では、核内フィラメントの数が著しく減少していることが明らかになった。また、Tprに対するsiRNA処理は、対照群のsiRNA処理細胞と比較して、細胞の成長と増殖を阻害した。Tprの減少した細胞ではp53とp21タンパク質の量が増加していた。驚くことに、Tprの減少はp53の核内での蓄積を増加させ、オートファジーを促進した。本研究は、TprがHSP70とHSF1のmRNAの核外輸送や、カリオフェリンCRM1によるp53の輸送に役割を担っていることを初めて示すものであり、これらはオートファジー因子の直接的な転写制御を介している可能性がある。
船坂 龍善1, 塚 恵利子1 & Richard W. Wong1, 2
- 金沢大学 理工研究域 自然システム学系 生物コース 分子細胞生物学研究室
- 金沢大学 理工研究域 バイオAFM先端研究センター
The nuclear pore complex (NPC) consists of a conserved set of ~30 different proteins, termed nucleoporins, and serves as a gateway for the exchange of materials between the cytoplasm and nucleus. Tpr (translocated promoter region) is a component of NPC that presumably localizes at intranuclear filaments. Here, we show that Tpr knockdown caused a severe reduction in the number of nuclear pores. Furthermore, our electron microscopy studies indicated a significant reduction in the number of inner nuclear filaments. In addition, Tpr siRNA treatment impaired cell growth and proliferation compared to control siRNA-treated cells. In Tpr-depleted cells, the levels of p53 and p21 proteins were enhanced. Surprisingly, Tpr depletion increased p53 nuclear accumulation and facilitated autophagy. Our study demonstrates for the first time that Tpr plays a role in autophagy through controlling HSP70 and HSF1 mRNA export, p53 trafficking with karyopherin CRM1, and potentially through direct transcriptional regulation of autophagy factors.

