Research Abstract
14-3-3γはMieapと相互作用してミトコンドリアの品質管理を行う
Identification of 14-3-3γ as a Mieap-interacting protein and its role in mitochondrial quality control
2012年4月24日 Scientific Reports 2 : 379 doi: 10.1038/srep00379
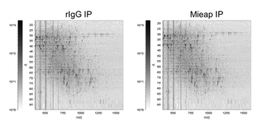
p53誘導性タンパク質であるMieapは、ミトコンドリア内へのリソソームタンパク質の集積を誘導することにより、ミトコンドリアの品質を管理する。この現象は、Mieapによるミトコンドリア内のリソソーム様オルガネラの集積誘導 [MALM(Mieap-induced accumulation of lysosome-like organelles within mitochondria)] と名付けられている。Mieapと相互作用する新規のタンパク質を同定するために、我々は抗Mieap抗体により免疫沈降したタンパク質に対して、2DICAL(two-dimensional image-converted analysis of liquid chromatography and mass spectrometry)を行った。その結果、MALM誘導時にMieap結合タンパク質複合体に含まれるタンパク質の一つとして、14-3-3γが同定された。Mieapと14-3-3γ間の相互作用は、外来性と内在性のタンパク質の両方で確認した。興味深いことに、MALMが起きたとき、14-3-3γはミトコンドリア内への局在を示した。14-3-3γの欠失は、ミトコンドリア内へのMieapやリソソームタンパク質の集積には影響しないが、酸化されたミトコンドリアタンパク質の除去を劇的に抑制した。これらの結果は、14-3-3γがミトコンドリア内でMieapとの相互作用を介して、MALMの過程における酸化されたミトコンドリアタンパク質の除去に重要な役割を担っていることを示唆している。
- 独立行政法人 国立がん研究センター研究所 腫瘍生物学分野
- 独立行政法人 国立がん研究センター研究所 創薬臨床研究分野
Mieap, a p53-inducible protein, controls mitochondrial integrity by inducing the accumulation of lysosomal proteins within mitochondria. This phenomenon is designated MALM, for Mieap-induced accumulation of lysosome-like organelles within mitochondria. To identify this novel Mieap-interacting protein(s), we performed a two-dimensional image-converted analysis of liquid chromatography and mass spectrometry (2DICAL) on the proteins immunoprecipitated by an anti-Mieap antibody. We indentified 14-3-3γ as one of the proteins that was included in the Mieap-binding protein complex when MALM was induced. The interaction between Mieap and 14-3-3γ was confirmed on the exogenous and endogenous proteins. Interestingly, 14-3-3γ was localized within mitochondria when MALM occurred. A 14-3-3γ deficiency did not affect the accumulation of Mieap and lysosomal proteins within mitochondria, but dramatically inhibited the elimination of oxidized mitochondrial proteins. These results suggest that 14-3-3γ plays a critical role in eliminating oxidized mitochondrial proteins during the MALM process by interacting with Mieap within mitochondria.

