TRIM29は損傷を受けたクロマチンへのDNA修復関連タンパク質の集積を調節する
TRIM29 regulates the assembly of DNA repair proteins into damaged chromatin
2015年6月22日 Nature Communications 6 : 7299 doi: 10.1038/ncomms8299
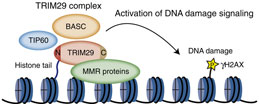
DNA二本鎖切断(DSB)修復は、DSB部位に集積した多数のタンパク質によって行われるが、DNA修復タンパク質が損傷を受けたクロマチンへ集合する仕組みは完全には解明されていなかった。本論文では、TRIM(tripartite motif)タンパク質ファミリーに属するTRIM29が、DNA損傷応答(DDR)を担うヒストン結合タンパク質であることを示す。TRIM29はBASC(BRCA1-associated surveillance complex)、コヒーシン、DNA-PKc群およびTIP60複合体の構成成分と相互作用することが分かった。H2AXヌクレオソーム上にあるTRIM29を含む複合体の動態は、ヒストン修飾間のクロストークによって調整される。ヌクレオソーム中では、TRIM29は修飾されたヒストンH3およびH4の尾部に結合する。また、電離放射線照射に対する応答の際に起こるTRIM29のクロマチンの結合は、H2AXリン酸化および細胞の生存に必要とされる。以上の結果は、TRIM29はDNA修復タンパク質がクロマチンに集積するための足場として機能し、それによってDDRが効率よく活性化されることを示唆している。
Yasushi Masuda, Hidehisa Takahashi, Shigeo Sato, Chieri Tomomori-Sato, Anita Saraf, Michael P. Washburn, Laurence Florens, Ronald C. Conaway, Joan W. Conaway & Shigetsugu Hatakeyama

