NarKによる硝酸イオン/亜硝酸イオン対向輸送機構の構造基盤
Structural basis for dynamic mechanism of nitrate/nitrite antiport by NarK
2015年5月11日 Nature Communications 6 : 7097 doi: 10.1038/ncomms8097
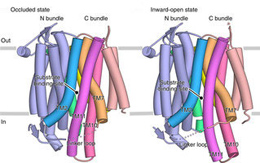
NarKは、二次性能動輸送体で最大のスーパーファミリーであるMFS(Major Facilitator Superfamily)中の硝酸イオン/亜硝酸イオン輸送体(NNP)ファミリーに属しており、細菌、古細菌、真菌、植物などの多様な生物における細胞膜を介しての硝酸イオン取り込みに中心的な役割を果たしている。これまでの研究から、NarKの全体構造や亜硝酸イオンの認識機構は明らかとなっていたが、硝酸イオン輸送の駆動力などを含めた基質輸送の分子機構についてはいまだ不明であった。今回我々は、NarKが硝酸イオン/亜硝酸イオン対向輸送体であることを人工的な脂質膜球(リポソーム)にNarKを再構成したアッセイ系を用いることでin vitroで実証した。さらに、大腸菌(Escherichia coli)由来のNarKについて、硝酸イオンが結合した閉じた状態、硝酸イオンが結合し内向きに開いた状態、および内向きに開いた基質非結合(apo)状態の3種類の結晶構造を高分解能で決定した。以上の構造解析、機能解析に、遺伝学的解析やコンピューターシミュレーションの結果も合わせて、本研究ではNarKによる硝酸イオン/亜硝酸イオン対向輸送の機構を明らかにした。すなわち、NarKの複数の膜貫通ヘリックスの構造変化と基質結合部位に位置する鍵となる重要なチロシン残基とアルギニン残基の構造変化が連動することで、基質認識が輸送サイクルと共役していることを突き止めた。
Masahiro Fukuda, Hironori Takeda, Hideaki E. Kato, Shintaro Doki, Koichi Ito, Andrés D. Maturana, Ryuichiro Ishitani & Osamu Nureki

