Research Abstract
タンパク質と脂質からなる細胞溶解性膜孔の自己組織化の構造基盤
Structural basis for self-assembly of a cytolytic pore lined by protein and lipid
2015年2月26日 Nature Communications 6 : 6337 doi: 10.1038/ncomms7337
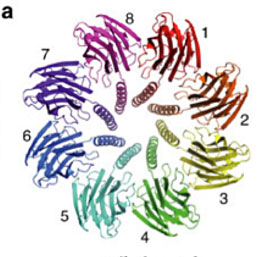
膜孔形成毒素(PFT)は水溶性のタンパク質として発現し、標的細胞の細胞膜上で自己組織化を起こして膜貫通小孔を形成するという注目すべき性質を備えており、こうした小孔は標的細胞に損傷を与える。今回我々は、αバレル型PFTである溶血毒素fragaceatoxin C(FraC)が細胞溶解を起こす過程でとる4つの状態、すなわち水溶性単量体、脂質の結合した単量体、自己組織化中間体および完全に組み立てられた膜貫通型小孔について、その結晶構造を決定し、それによってFraCの作用機序を解明した。膜を貫通する小孔は、タンパク質と脂質の両方から構成された特徴的な構造を有していた。この中で、小孔内壁に並んだ脂質は小孔構築の共因子として働いていることが分かった。またこの小孔には側方に開口部があり細胞膜の疎水性コアが水溶液環境に露出している。小孔の構造内に標的膜の脂質を取り込むことが、膜特異的に溶血毒素を活性化するための引き金となっている。
Koji Tanaka, Jose M.M. Caaveiro, Koldo Morante, Juan Manuel González-Mañas & Kouhei Tsumoto
Corresponding Author
Pore-forming toxins (PFT) are water-soluble proteins that possess the remarkable ability to self-assemble on the membrane of target cells, where they form pores causing cell damage. Here, we elucidate the mechanism of action of the haemolytic protein fragaceatoxin C (FraC), a α-barrel PFT, by determining the crystal structures of FraC at four different stages of the lytic mechanism, namely the water-soluble state, the monomeric lipid-bound form, an assembly intermediate and the fully assembled transmembrane pore. The structure of the transmembrane pore exhibits a unique architecture composed of both protein and lipids, with some of the lipids lining the pore wall, acting as assembly cofactors. The pore also exhibits lateral fenestrations that expose the hydrophobic core of the membrane to the aqueous environment. The incorporation of lipids from the target membrane within the structure of the pore provides a membrane-specific trigger for the activation of a haemolytic toxin.

