TRPV2はマウスで心臓の構造と機能の維持に必須である
TRPV2 is critical for the maintenance of cardiac structure and function in mice
2014年5月29日 Nature Communications 5 : 3932 doi: 10.1038/ncomms4932
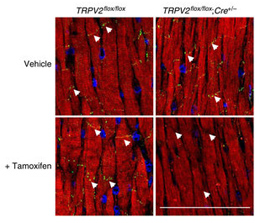
心臓は、運動や加齢などで生じる血行動態の変化に対して、形や機能を変えて適応する能力を備えている。しかしながら、心臓の機械刺激受容機構は明らかにされていない。本論文では、TRPV2(transient receptor potential, vanilloid family type 2)陽イオンチャネルが心臓の構造と機能の維持に必須であることを示す。成体マウスの心臓からTRPV2を除去すると、その4日後以内に重篤な心機能低下が見られ、隣接する心筋細胞間の機械的共役を支える介在板の構造が崩れ、その後心筋細胞同士の電気的連絡も弊害され、心筋での刺激伝導が障害される。9日目以降になると、TRPV2欠失心臓の単一心筋細胞では、収縮力の低下と、これを支えるCa2+ハンドリングが障害されていた。TRPV2を欠く新生仔心筋細胞では、介在板形成が弊害されており、伸展刺激依存的な細胞内Ca2+の上昇や、インスリン様増殖因子(IGF-1)分泌が見られなくなった。さらに、TRPV2を欠失する心臓ではIGF-1受容体/PI3K/Akt経路のシグナル伝達分子の発現が著しく低下していた。このような心臓へのIGF-1投与は、TRPV2欠損によって生じる心室の拡大と心臓ポンプ機能障害を部分的に防止した。我々の結果は、拍動によって常に動き続けている心臓の構造と機能の維持の基盤となる分子過程の理解を進めるものである。
片野坂 友紀1, 岩崎 慶一朗1, 氏原 嘉洋1,2, 高津 理美1, 西辻 光希1, 金川 基3, 首藤 篤史3, 戸田 達史3, 片野坂 公明4,5, 毛利 聡1,2 & 成瀬 恵治1,6
- 岡山大学大学院 医歯学総合研究科 システム生理学
- 川崎医科大学 生理学1
- 神戸大学大学院 医学研究科 分子脳科学
- 名古屋大学 環境医学研究所 神経系分野2
- 中部大学 生命健康科学部 生命医科学科
- JST戦略的創造研究推進事業 発展研究(ICORP-SORST)

