Research Abstract
無機リン酸解離のタイミングは、ATPで駆動する回転モータータンパク質の触媒活性を制御している
Timing of inorganic phosphate release modulates the catalytic activity of ATP-driven rotary motor protein
2014年4月1日 Nature Communications 5 : 3486 doi: 10.1038/ncomms4486
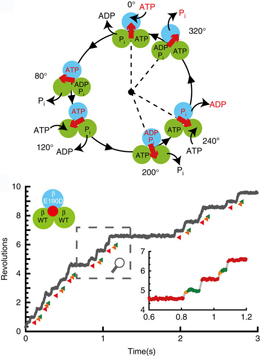
F1-ATPaseは、ATPの加水分解で得られるエネルギーを利用して回転するモータータンパク質である。F1-ATPaseの回転運動は触媒反応と強く共役しており、また、触媒反応のスキームは素過程単位で厳密に制御されている。このような反応スキームの厳密な制御は、F1-ATPaseの特徴である化学・力学間の高いエネルギー変換効率およびそれらの可逆的な変換を実現するのに重要と考えられている。そこで、本論文では、1分子操作によって反応スキームを意図的に変化させ、それがF1-ATPaseの回転運動に及ぼす影響を調べた。反応生成物であるADPと無機リン酸が解離する順番を入れ換えると、F1-ATPaseが頻繁にかつ長時間にわたり回転運動を停止させる現象(= 触媒反応における不活性化)が観察された。この不活性状態はMgADP阻害状態の性質を表しており、すなわち、F1-ATPaseでは触媒反応のスキームが不適切だとMgADP阻害状態が引き起こされることが分かった。
渡邉 力也1,2 & 野地 博行1
- 東京大学大学院 工学系研究科 応用化学専攻
- 独立行政法人 科学技術振興機構 さきがけ
F1-ATPase is a rotary motor protein driven by ATP hydrolysis. The rotary motion of F1-ATPase is tightly coupled to catalysis, in which the catalytic sites strictly obey the reaction sequences at the resolution of elementary reaction steps. This fine coordination of the reaction scheme is thought to be important to achieve extremely high chemomechanical coupling efficiency and reversibility, which is the prominent feature of F1-ATPase among molecular motor proteins. In this study, we intentionally change the reaction scheme by using single-molecule manipulation, and we examine the resulting effect on the rotary motion of F1-ATPase. When the sequence of the products released, that is, ADP and inorganic phosphate, is switched, we find that F1 frequently stops rotating for a long time, which corresponds to inactivation of catalysis. This inactive state presents MgADP inhibition, and thus, we find that an improper reaction sequence of F1-ATPase catalysis induces MgADP inhibition.

