Research Abstract
ミドリムシの4回膜貫通型タンパク質IP39は非対称な三量体を最小繰り返し単位とする線状重合体を形成する
The four-transmembrane protein IP39 of Euglena forms strands by a trimeric unit repeat
2013年4月23日 Nature Communications 4 : 1766 doi: 10.1038/ncomms2731
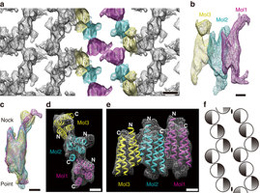
ミドリムシ類の細胞膜には縞状の表面構造(ペリクル)が見られ、ユーグレナ運動と呼ばれる鞭毛虫に特徴的な運動の際には、この構造体がスライドすることで細胞全体のダイナミックな変形運動が可能になっている。ミドリムシ(Euglena gracilis)では、主要な内在性膜タンパク質であるIP39が高密度かつ規則的に配列してペリクル膜を覆っている。IP39は、PMP-22/EMP/MP20/Claudinスーパーファミリーの保存された配列モチーフを持つ4回膜貫通型タンパク質であると考えられている。本論文では、電子線結晶構造解析によって決定したミドリムシIP39の三次元構造を報告する。脂質膜中でIP39は、三量体を最小単位として縦方向に重合した逆平行2本鎖を形成し、それが真っすぐ伸びたジグザグの線状構造をとっていた。この構造解析から、三量体内におけるIP39の非対称的な分子配置が明らかになり、隣接するプロトマー間には少なくとも4種類の相互作用が存在することが示された。このような複数の分子間相互作用の組み合わせが、脂質二重層内で膜タンパク質が直線状のストランドを形成する際に重要だと考えられる。
鈴木 博視1, 伊藤 泰行2,3, 山崎 裕自2, 峯田 克彦4, 氏 昌未2, 阿部 一啓1, 谷 一寿1, 藤吉 好則1 & 月田 早智子2
- 名古屋大学 細胞生理学研究センター(CeSPI)
- 大阪大学大学院 生命機能研究科
- 日本学術振興会 特別研究員
- 北海道大学大学院 情報科学研究科
Euglenoid flagellates have striped surface structures comprising pellicles, which allow the cell shape to vary from rigid to flexible during the characteristic movement of the flagellates. In Euglena gracilis, the pellicular strip membranes are covered with paracrystalline arrays of a major integral membrane protein, IP39, a putative four-membrane-spanning protein with the conserved sequence motif of the PMP-22/EMP/MP20/Claudin superfamily. Here we report the three-dimensional structure of Euglena IP39 determined by electron crystallography. Two-dimensional crystals of IP39 appear to form a striated pattern of antiparallel double-rows in which trimeric IP39 units are longitudinally polymerised, resulting in continuously extending zigzag-shaped lines. Structural analysis revealed an asymmetric molecular arrangement in the trimer, and suggested that at least four different interactions between neighbouring protomers are involved. A combination of such multiple interactions would be important for linear strand formation of membrane proteins in a lipid bilayer.

