Research Abstract
胃酸抑制剤によって誘導される胃H+,K+-ATPアーゼのコンフォメーション変化
本論文では、代表的なK+拮抗ブロッカーであるSCH28080が、胃H+,K+-ATPアーゼに結合した複合体の立体構造を7 Å分解能で解析した結果について報告する。
Conformational rearrangement of gastric H,K-ATPase induced by an acid suppressant
2011年1月11日 Nature Communications 2 : 155 doi: 10.1038/ncomms1154
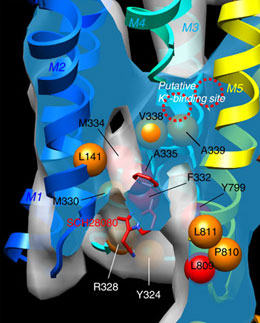
胃酸に関連した疾患は消化管の酸性化異常に関係している。胃のプロトンポンプであるH+,K+-ATPアーゼはH+とK+の対抗輸送によって胃内腔に非常に酸性度の高い環境を作り出しており、そのために胃酸抑制剤の主な標的となっている。本論文では、代表的なK+拮抗ブロッカーであるSCH28080が、胃H+,K+-ATP アーゼに結合した複合体の立体構造を7 Å分解能で解析した結果について報告する。これは二次元結晶を作製して、電子線結晶学という方法を用いて解析された。結合したSCH28080は、膜貫通 (TM)へリックス4、5および6の近傍の管腔側キャビティ内に見られる。SCH28080の結合部位は、TMへリックスの再配置によって形成され、この 変化は細胞質側のドメインにも伝わり、その結果管腔側に開いたコンフォメーションが形成される。今回の結果は、H+,K+-ATPアーゼ上の胃酸抑制剤結合部位についての最初の構造学的証拠であり、この種の薬剤によって誘導されるコンフォメーション変化を明らかにしている。
- 京都大学大学院 理学研究科
Acid-related gastric diseases are associated with disorder of digestive tract acidification. The gastric proton pump, H+,K+-ATPase, exports H+ in exchange for luminal K+ to generate a highly acidic environment in the stomach, and is a main target for acid suppressants. Here, we report the three-dimensional structure of gastric H+,K+-ATPase with bound SCH28080, a representative K+-competitive acid blocker, at 7 Å resolution based on electron crystallography of two-dimensional crystals. The density of the bound SCH28080 is found near transmembrane (TM) helices 4, 5 and 6, in the luminal cavity. The SCH28080-binding site is formed by the rearrangement of TM helices, which is in turn transmitted to the cytoplasmic domains, resulting in a luminal-open conformation. These results represent the first structural evidence for a binding site of an acid suppressant on H+,K+-ATPase, and the conformational change induced by this class of drugs.

