AAVベクターの生後投与を介したCRISPR/Cas9ゲノム編集により血友病Bマウスを治療
CRISPR/Cas9-mediated genome editing via postnatal administration of AAV vector cures haemophilia B mice
2017年6月23日 Scientific Reports 7 : 4159 doi: 10.1038/s41598-017-04625-5
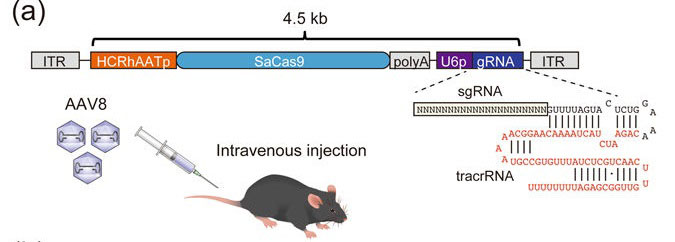
血友病Bは、凝固第IX因子遺伝子(F9)の変異によって引き起こされる先天性出血性疾患で、ゲノム編集技術による治療に適した疾患であると考えられている。本論文では、CRISPR(clustered regularly interspaced short palindromic repeat)/Cas9系を用いて、生後の血友病Bマウスを治療するための戦略を報告する。黄色ブドウ球菌(Staphylococcus aureus)のCas9(SaCas9)と単一ガイドRNA(sgRNA)を組み込んだアデノ随伴ウイルス(AAV)8ベクターを成体の野生型マウスに投与すると、肝細胞のF9の標的部位に二本鎖切断(DSB)が誘導され、血中凝固第IX因子が血友病Bのレベルまで低下した。これと同時に相同組換え修復(HDR)を発現させることで変異特異的な遺伝子編集を行うと、FIXレベルが上昇し、疾患表現型(出血傾向)が修正された。DSBに続いて、非相同末端結合(NHEJ)およびHDRの両方の過程を介してイントロンにF9 cDNAが挿入されると、より効率的に止血機能が回復した。これらのゲノム編集による治療は、従来のAAVベクターを用いた遺伝子治療では困難である新生仔マウスの治癒も行うことができた。アンチトロンビン遺伝子を標的とするアンチセンスオリゴヌクレオチドを用いた血友病治療が報告されているが、この治療はSaCas9/sgRNAを発現するAAV8ベクターでも可能である。我々の結果は、AAV8ベクターを用いたCRISPR/Cas9ゲノム編集が、肝細胞において標的遺伝子にDSBを誘導する柔軟性のある手法であり、また、血友病の遺伝子治療のための優れた戦略である可能性を示している。
Corresponding Author
Haemophilia B, a congenital haemorrhagic disease caused by mutations in coagulation factor IX gene (F9), is considered an appropriate target for genome editing technology. Here, we describe treatment strategies for haemophilia B mice using the clustered regularly interspaced short palindromic repeat (CRISPR)/Cas9 system. Administration of adeno-associated virus (AAV) 8 vector harbouring Staphylococcus aureus Cas9 (SaCas9) and single guide RNA (sgRNA) to wild-type adult mice induced a double-strand break (DSB) at the target site of F9 in hepatocytes, sufficiently developing haemophilia B. Mutation-specific gene editing by simultaneous induction of homology-directed repair (HDR) sufficiently increased FIX levels to correct the disease phenotype. Insertion of F9 cDNA into the intron more efficiently restored haemostasis via both processes of non-homologous end-joining (NHEJ) and HDR following DSB. Notably, these therapies also cured neonate mice with haemophilia, which cannot be achieved with conventional gene therapy with AAV vector. Ongoing haemophilia therapy targeting the antithrombin gene with antisense oligonucleotide could be replaced by SaCas9/sgRNA-expressing AAV8 vector. Our results suggest that CRISPR/Cas9-mediated genome editing using an AAV8 vector provides a flexible approach to induce DSB at target genes in hepatocytes and could be a good strategy for haemophilia gene therapy.

