ラミニン断片をコーティングしないで用いるヒト多能性幹細胞の効率的な接着培養
Efficient Adhesion Culture of Human Pluripotent Stem Cells Using Laminin Fragments in an Uncoated Manner
2017年1月30日 Scientific Reports 7 : 41165 doi: 10.1038/srep41165
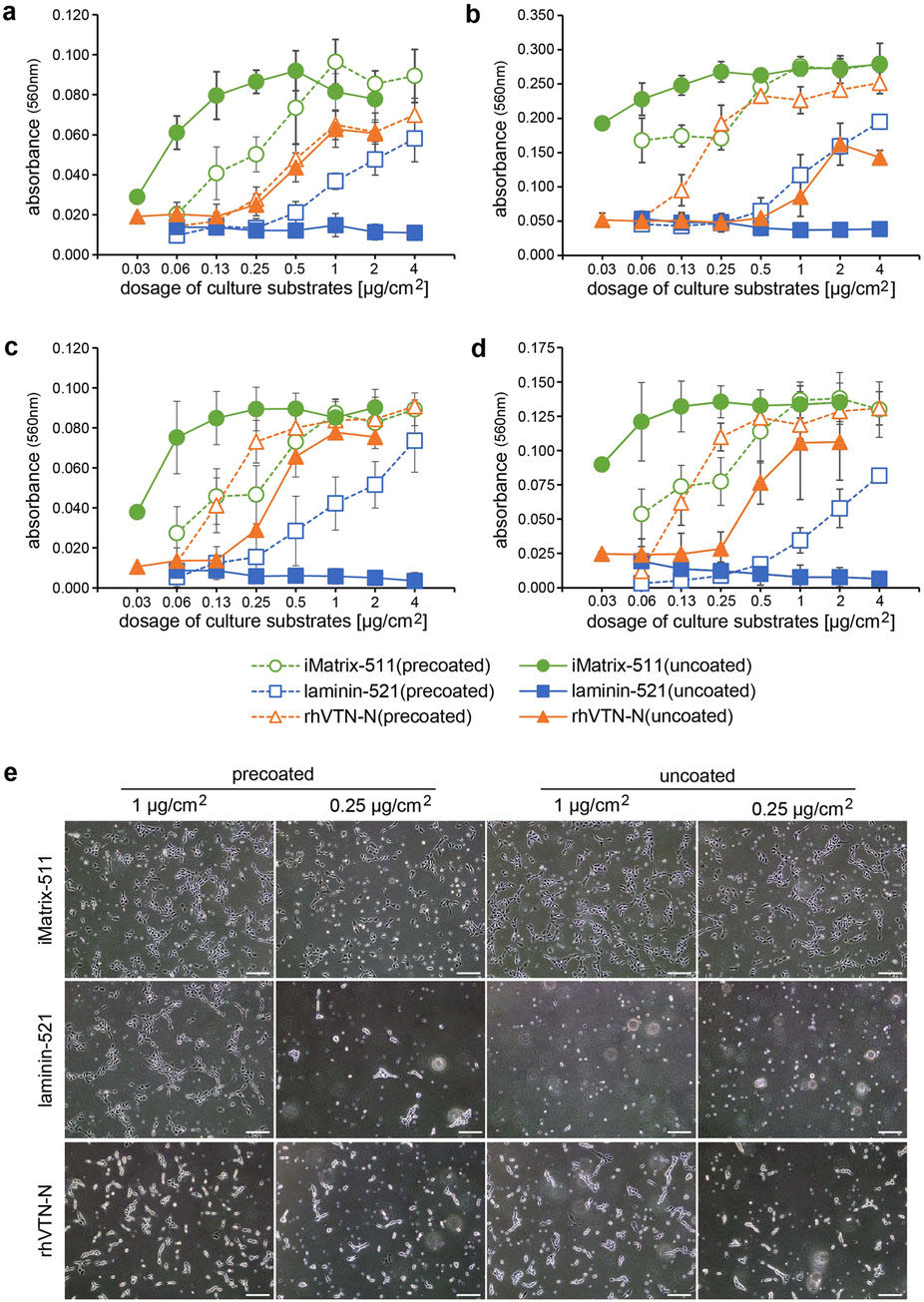
我々は、ラミニン断片をプレコーティングすることなく、ヒト多能性幹細胞(hPSC)を非常に効率的に接着培養する方法について報告する。培養基質は一般的に、培養容器に予めコーティングすることにより、細胞接着効果を発揮すると考えられている。しかし、細胞を継代する際に細胞浮遊液にラミニン断片を添加するだけで、培養基質のプレコーティングを行っていない培養容器に、分離させた単一のhPSCの接着を促すことができた。ラミニン断片をプレコーティングする従来の前処理と同様に、ラミニン断片を添加することで、単一hPSCのロバストな接着を支持でき、また、プレコーティングと比較して、この方法ではより低濃度で最大の接着効果を示したことは興味深い。ラミニン断片をプレコーティングと同様に、コーティングすることなく添加することで、hPSCの接着性は高まり、培養容器から剥がれることなく、良好な増殖を示し、また継続的な継代培養後も多能性を維持していた。完全長ラミニンやビトロネクチンなど、他の培養基質が、コーティングしない方法でhPSCの接着を支持するかどうかを検討したが、ラミニン断片のみがコーティングしない方法で用いることができた。この費用効率と時間効率の高い方法は、hPSCの拡大培養に寄与し、また、hPSCを用いる再生医療の開発を加速する可能性がある。
Corresponding Author
We describe highly effective adhesion culture of human pluripotent stem cells (hPSCs) using laminin fragments without precoating. Culture substrates have been generally thought to exert a cell adhesion effect when they are precoated onto culture vessels. However, simple addition of laminin fragments to a cell suspension during passaging accelerated the adhesion of single dissociated hPSCs onto culture vessels that were not precoated with any culture substrate. Interestingly, similar to conventional precoating, the uncoated addition of laminin fragments supported robust adhesion of single hPSCs and maximum adhesion at a much lower concentration compared with precoating. Similar to precoating laminin fragments, hPSCs seeded with uncoated laminin fragments grew well without cell detachment and maintained pluripotency after continuous subculture. We tested other culture substrates, including full-length laminin and vitronectin, to support hPSC adhesion in the uncoated manner, but only laminin fragments had the potential for application in the uncoated manner. This cost-effective and time-efficient method may contribute to expansion of culture of hPSCs and accelerate the development of regenerative medicine using hPSCs.

