マイクロRNA-302スイッチを用いた未分化なヒト多能性幹細胞の同定および除去
MicroRNA-302 switch to identify and eliminate undifferentiated human pluripotent stem cells
2016年9月9日 Scientific Reports 6 : 32532 doi: 10.1038/srep32532
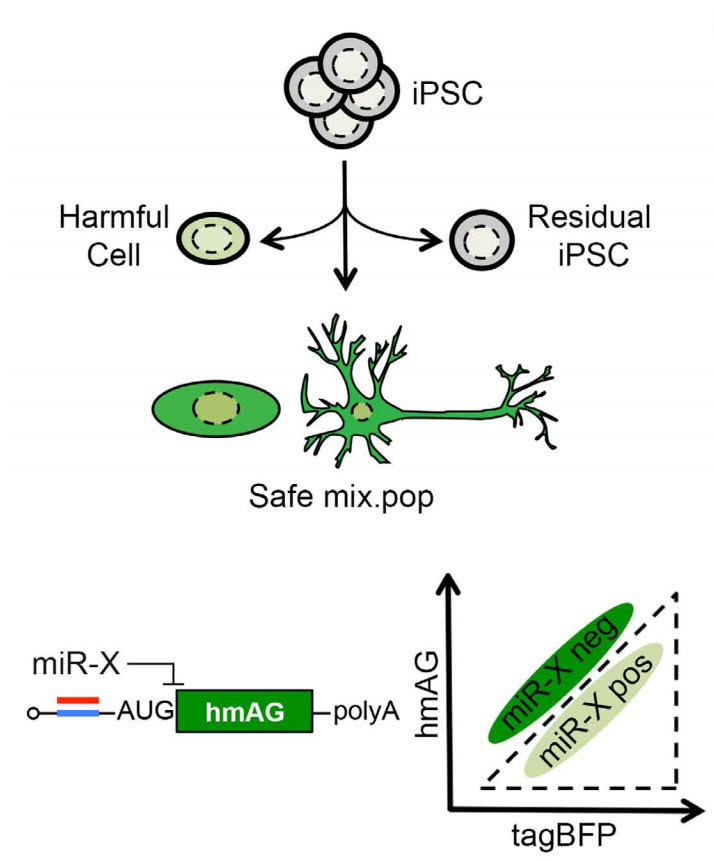
多能性幹細胞からの分化誘導効率には非常にばらつきがあるので、未分化な細胞を含む不均一な細胞集団が生じることが多い。今回我々は、移植の前に望まない細胞を除去するための、感度が高く、標的特異的で、一般的な方法を開発したことを報告する。マイクロRNA-302a-5p(miR-302a)はヒト多能性幹細胞で特異的に高い活性が見られ、分化過程で基底レベルまで徐々に活性が低下する。我々は、新しいRNAツールとして、生細胞においてmiR-302a活性を検知できるレポーターmRNA、「miR-302aスイッチ」を合成した。このmiR-302aスイッチは、特異的にヒト誘導多能性幹細胞(hiPSC)を検出でき、不均一な細胞集団に含まれるhiPSCが0.05%のレベルまで検出が可能であった。また混合細胞集団にmiR-302aスイッチを導入した後に、in vivo腫瘍形成能を評価すると、奇形腫の形成が阻止できた。さらに、miR-302aの活性に応じてピューロマイシン耐性遺伝子の発現を制御するスイッチを用いることで、hiPSCを自動かつ選択的に除去することを達成した。我々の系は、多能性幹細胞や部分的に分化した細胞を高感度で検出する独自の方法である。miR-302aスイッチは、未分化細胞を除去する能力に加えて、細胞内の情報に基づき、生細胞の分化および/あるいは再プログラム化の動態を調べる際にも大きな可能性を秘めている。
Corresponding Author
The efficiency of pluripotent stem cell differentiation is highly variable, often resulting in heterogeneous populations that contain undifferentiated cells. Here we developed a sensitive, target-specific, and general method for removing undesired cells before transplantation. MicroRNA-302a-5p (miR-302a) is highly and specifically expressed in human pluripotent stem cells and gradually decreases to basal levels during differentiation. We synthesized a new RNA tool, miR-switch, as a live-cell reporter mRNA for miR-302a activity that can specifically detect human induced pluripotent stem cells (hiPSCs) down to a spiked level of 0.05% of hiPSCs in a heterogeneous population and can prevent teratoma formation in an in vivo tumorigenicity assay. Automated and selective hiPSC-elimination was achieved by controlling puromycin resistance using the miR-302a switch. Our system uniquely provides sensitive detection of pluripotent stem cells and partially differentiated cells. In addition to its ability to eliminate undifferentiated cells, miR-302a switch also holds great potential in investigating the dynamics of differentiation and/or reprograming of live-cells based on intracellular information.

