Research Abstract
ヒト骨髄由来のヒト間葉系幹細胞はある一定周波数以上の機械的ストレスを与えると多能性を保ったままで増殖が抑制される
Frequent mechanical stress suppresses proliferation of mesenchymal stem cells from human bone marrow without loss of multipotency
2016年4月15日 Scientific Reports 6 : 24264 doi: 10.1038/srep24264
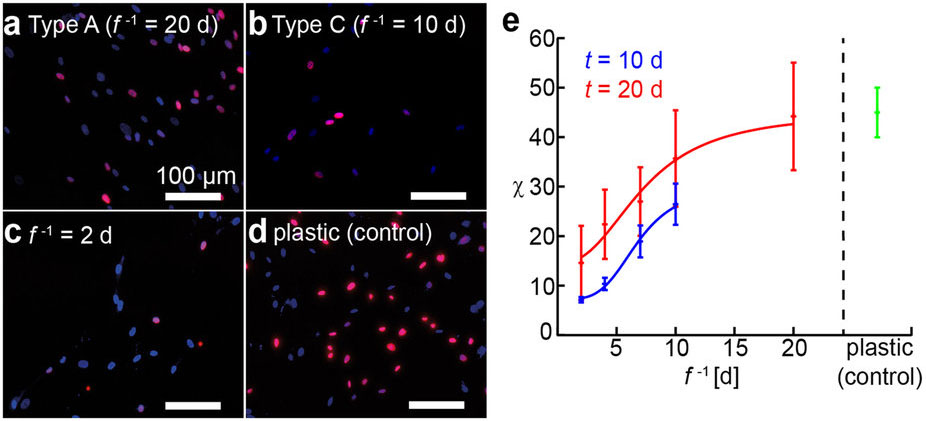
近年多くの研究が、骨髄由来のヒト間葉系幹細胞(hMSC)の分化が生化学的な要素だけでなく、基板のトポグラフィーや剛性などの物理的微小環境にも影響を受けることを示してきた。筆者らは「生きた(in vivo)」骨髄内の幹細胞微小環境が動的に制御されていることに注目し、従来型の共有結合で化学架橋されたヒドロゲルに代わって、基板の硬さ(弾性率)を微小な化学刺激により自在に変えられる、物理架橋した生体適合性ヒドロゲル材料を新たに考案した。このヒドロゲル基板上で増殖させたhMSCは、基板の弾性率に関わらず、20日にわたり多分化能マーカーであるSTRO-1の発現を90%以上維持した。この培養hMSCを脂肪や骨分化を誘導する培養液に移すと、脂肪細胞や骨芽細胞へと分化をした。興味深いことに、基板の弾性を変化させる周期を短くしていくと幹細胞は多分化能を保ったままで増殖が顕著に減少した。たとえば1日おきに基板の硬さを変化させた基板上ではhMSCの増殖は最大90%まで抑制された。このような「動的in vitro幹細胞ニッチ」はhMSCの運命に与える動的な力学的ストレスの役割を明らかにするのに応用できるだけでなく、幹細胞をin vitroで同期化した上で分化誘導する技術基盤となることが期待できる。
Corresponding Authors
Mounting evidence indicated that human mesenchymal stem cells (hMSCs) are responsive not only to biochemical but also to physical cues, such as substrate topography and stiffness. To simulate the dynamic structures of extracellular environments of the marrow in vivo, we designed a novel surrogate substrate for marrow derived hMSCs based on physically cross-linked hydrogels whose elasticity can be adopted dynamically by chemical stimuli. Under frequent mechanical stress, hMSCs grown on our hydrogel substrates maintain the expression of STRO-1 over 20 d, irrespective of the substrate elasticity. On exposure to the corresponding induction media, these cultured hMSCs can undergo adipogenesis and osteogenesis without requiring cell transfer onto other substrates. Moreover, we demonstrated that our surrogate substrate suppresses the proliferation of hMSCs by up to 90% without any loss of multiple lineage potential by changing the substrate elasticity every 2nd days. Such “dynamic in vitro niche” can be used not only for a better understanding of the role of dynamic mechanical stresses on the fate of hMSCs but also for the synchronized differentiation of adult stem cells to a specific lineage.

