マウス半数体胚性幹細胞でのCRISPR/Cas9を介したレポーターのノックイン
CRISPR/Cas9-mediated reporter knock-in in mouse haploid embryonic stem cells
2015年6月3日 Scientific Reports 5 : 10710 doi: 10.1038/srep10710
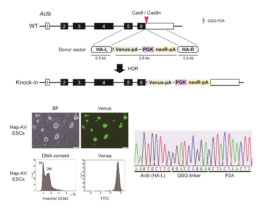
マウス雌性半数体の胚性幹細胞は、化学的に活性化された卵母細胞から単為発生で得られる多能性幹細胞である。半数体の細胞は、ゲノムを1組しか持たないため、遺伝子変化の影響を研究する強力なツールとなる。しかし、細胞分化などの生物学的過程をモニターする理想的なレポーターがないため、目的の表現型を持つ細胞を選び出すことには限界があった。 今回我々は、CRISPR/Cas9を用いて、マウス半数体胚性幹細胞の標的遺伝子を破壊せずに、レポーターカセットをノックインする方法を確立したので報告する。最初に、P2A-Venusレポーターをハウスキーピング遺伝子座に挿入することで、この系の有効性を確認した。Cas9ヌクレアーゼを用いる従来の戦略に加えて、標的外への変異誘発を減少させることができるCas9ニッカーゼおよび短縮型ガイドRNAでもノックインが可能であり、高いガイド活性を持つガイドRNAを用いた場合に、高いノックイン効率がみられる傾向があった。次に、神経マーカー遺伝子Sox1の下流にP2A-Venusレポーターを挿入し、神経分化をモニターすることでレポーターの有用性を確認した。我々のデータは、CRISPR/Cas9を介したノックイン系を用いることで、任意の遺伝子特異的レポーターをノックインした半数体胚性幹細胞株を樹立できることを示している。遺伝子編集された半数体胚性幹細胞は、発生経路の順遺伝学的スクリーニングなどに応用できる可能性がある。
Yasuyoshi Kimura, Masaaki Oda, Tsunetoshi Nakatani, Yoichi Sekita, Asun Monfort, Anton Wutz, Hideki Mochizuki & Toru Nakano

