Research Abstract
ホスミドマイシンがヒト熱帯熱マラリア原虫(Plasmodium falciparum)へ及ぼす作用の分子的基盤
Molecular basis of fosmidomycin's action on the human malaria parasite Plasmodium falciparum
2011年6月14日 Scientific Reports 1 : 9 doi: 10.1038/srep00009
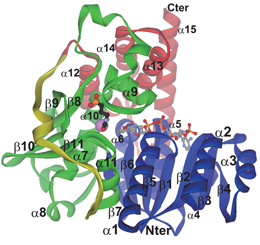
ヒトに感染する熱帯熱マラリア原虫(Plasmodium falciparum)は、毎年100万人以上の感染者を死に至らしめている。ホスミドマイシンは、ヒトには存在しない代謝経路である非メバロン酸経路の酵素1-デオキシ-D-キシルロース-5-リン酸レダクトイソメラーゼ(DXR)を阻害することで原虫の増殖を抑制し、熱帯熱マラリアの治療におけるその有効性が実証されている。しかし、熱帯熱マラリア原虫にホスミドマイシンが及ぼすDXR阻害の構造的機序の詳細は明らかにされていない。今回我々は、ホスミドマイシンが結合したPfDXRの完全四成分構造複合体の結晶構造について報告する。我々の研究は、(i) PfDXR分子の柔軟性が活性部位において阻害剤を収納する際に生じる誘導適合を説明付け、(ii) 結合阻害剤のヒドロキサム酸基における酸素原子のシス配列が、活性部位の金属と阻害剤との強固な結合に必須であることを明らかにしている。我々は、この構造がさらに有効な抗マラリア薬の薬剤デザインを行う際に有用な手がかりとなることを期待する。
- 昭和大学 薬学部
- 松山大学 薬学部
- 岐阜大学 工学部
- 岐阜大学 先端創薬研究センター
- 岐阜大学 人獣感染防御研究センター
- 岐阜大学大学院 連合創薬医療情報研究科
The human malaria parasite Plasmodium falciparum is responsible for the deaths of more than a million people each year. Fosmidomycin has been proven to be efficient in the treatment of P. falciparum malaria by inhibiting 1-deoxy-D-xylulose 5-phosphate reductoisomerase (DXR), an enzyme of the non-mevalonate pathway, which is absent in humans. However, the structural details of DXR inhibition by fosmidomycin in P. falciparum are unknown. Here, we report the crystal structures of fosmidomycin-bound complete quaternary complexes of PfDXR. Our study revealed that (i) an intrinsic flexibility of the PfDXR molecule accounts for an induced-fit movement to accommodate the bound inhibitor in the active site and (ii) a cis arrangement of the oxygen atoms of the hydroxamate group of the bound inhibitor is essential for tight binding of the inhibitor to the active site metal. We expect the present structures to be useful guides for the design of more effective antimalarial compounds.

