微小管βチューブリンタンパク質が神経疾患を引き起こすメカニズムが明らかに
武藤 悦子、箕浦 逸史
2016年1月18日掲載
眼筋麻痺による斜視や眼瞼下垂を主な症状とする先天性外眼筋繊維症(CFEOM)。CFEOMは1型、2型、3型に分類され、3型(CFEOM3)は、微小管形成の阻害による脳神経の発生異常、特に神経軸索の形成不全が原因と考えられている。微小管を構成するタンパク質βチューブリンの遺伝子変異が微小管形成の異常を引き起こすメカニズムを明らかにした1、理化学研究所脳科学総合研究センター所属の武藤悦子チームリーダーと箕浦逸史研究員に、今回の研究成果や今後の展望について話を聞いた。
―― 微小管・チューブリンとは?
箕浦氏: 微小管は、細胞の骨格として、アクチンと並んで細胞の形を決定するのに重要な役割を担っています。微小管を構成するチューブリンと呼ばれるタンパク質は、全ての真核細胞が持っており、地球上で生命が進化しても種を超えて保存されてきました。またチューブリンは、神経細胞の形成や維持にも極めて重要な役割を果たしています。
武藤氏: 私は、理化学研究所の和光地区で研究室を15年前に立ち上げて以来、ずっと、微小管を研究してきました。微小管はサイズが大きいので、精製したものを光学顕微鏡で直接観察することができます。長年見ていると、その時々で微妙に違う微小管の“表情”が読み取れるようになってきて、生き物のようで、とても面白いんですよ。研究室に新たに着任した研究員は半年もすると、顕微鏡を見ながら「今日の微小管は“元気が良い”」などと言うようになります。
箕浦氏: 微小管を構成するチューブリンには、αチューブリン、βチューブリンがあり、ヒトでは8種類の異なるβチューブリン遺伝子があります。異なるチューブリンで構成される微小管は、物理的な特性も違います。チューブリンの構造の違いによって、微小管の構造が変わるためです。
武藤氏: 微小管は、分子の挙動を実際に「見る」ことができるため、研究対象として非常に魅力的です。分子生物学的な手法が使えるようになったおかげで、現象論だけで終わることなく、今や、そのメカニズムまで調べられるようになりました。
我々は、組換えチューブリンを発現・精製する技術を10年がかりで開発してきました。生命の仕組みを、細胞や個体レベルで研究して行く方法もありますが、in vitroで分子レベルから攻めて、それをin vivoでしっかりと検証できたことが今回の成功につながったと思います。
―― 今回の研究について。
武藤氏: 今回の研究は、「ヒトβ3チューブリンタンパク質の262番目にあるアルギニン残基(R262)がどのように疾患に関係しているのか」という疑問から始まりました。微小管に沿って、モータータンパク質がさまざまな物質を輸送することで神経が正常に形成されますが、その仕組みが正常に働かなくなっているのではないかと考えました。
箕浦氏: 我々はこの疑問について調べるために、β3チューブリンやモータータンパク質であるキネシンについて、さまざまな組換えタンパク質を作りました。こうして作ったβ3チューブリンのR262変異体が、キネシンと相互作用できず、キネシンの正常な運動を妨げることを突き止めました。
また、このR262変異体によって起こる異常を回復できる、キネシンの変異体も見つけることができました。このキネシンの「レスキュー変異体」は、β3チューブリンR262変異体で構成されている微小管に結合して、正常な運動を行うことができるのです。
一方、マウス胎仔の脳に、β3チューブリンR262変異体を発現する遺伝子を導入したところ、脳梁と呼ばれる、左右の脳をつなぐ神経繊維が短くなることが分かりました。
武藤氏: 脳梁の形成不全は、CFEOM3の患者で実際に見られる症状です。β3チューブリンとキネシンの相互作用がうまくいかないために微小管の形成が妨げられ、神経が正常に伸びて配線されなかったと考えられます。
箕浦氏: ところが同じマウスの脳で、キネシンのレスキュー変異体を、β3チューブリン変異体と一緒に発現させると、脳梁の神経繊維の長さはほぼ正常に戻りました。β3チューブリンとキネシンとの相互作用が、神経軸索の正しい形成のために必要不可欠であると示すことができたわけです。
武藤氏: レスキュー機構まで解明できたのは、箕浦さんをはじめとしてチーム全員の努力の賜物です。
―― 今後の展望は?
箕浦氏: 微小管やβ3チューブリンタンパク質について、さらに調べていきたいと思っています。抗がん剤の中には微小管を標的としているものがいくつかあり、抗がん剤創薬分野への応用が期待されます。また、β3チューブリンを持っているのは生物の中でも哺乳類だけであることから、哺乳類の複雑な神経系の発達には、このβ3チューブリンが重要な役割を果たしてきたのではないかと想像しています。今回の知見から、哺乳類の神経系が進化してきた過程を理解する手掛かりが得られるようになるかもしれません。
―― Nature Communications に投稿するまでの経緯は?
武藤氏: チューブリンタンパク質の発現系について最初の速報は、2013年のFEBS Letters2)にパブリッシュしました。その際、国内外のたくさんの研究者が私たちの論文に強い関心を示してくれたことが自信になり、前回の論文の延長線上にある今回の成果は、Nature Communications に投稿することを決めました。
箕浦氏: Nature Communications は総合科学ジャーナルですので、生物物理学、生化学、神経科学にかぎらず、さまざまな研究分野の人に読んでもらえるのは魅力ですね。しかし、幅広い読者に読んでもらうためには、書き方も内容も高いレベルを求められました。分子メカニズムの発見だけではインパクトが弱く、マウスを使ったin vivoでの実験結果を基に、疾患の理解や治療につながる可能性など、内容をより豊かにする必要がありました。
武藤氏: オープンアクセスというのも大きなメリットです。今、日本でも文部科学省を中心にオープンアクセスを推進する動きが随分と進められていますが、オープンアクセスの必要性やメリットは以前から感じていました。
―― Nature Communications に投稿してみて。
箕浦氏: 査読結果のコメントやアドバイスを読むと、エディターが、我々の研究内容をよく分かってくれている印象を受けました。特に、査読者からのコメントに対して、「このコメントはマイナーな点だから、そこまで気にしなくても良い」「このコメントは大事な提案なので改訂したほうがよい」といったふうに、改訂の方針を提案してくれたのでとても助かりました。
武藤氏: 査読のスピードも早かったですね。今回の論文はアクセプトされるまでに2回の改訂を行いましたが、原稿を提出してからその結果が返ってくるまでの期間は短かったと思います。改訂の際に求められたデータの作成には苦労しましたが。研究データの検証をするために細胞培養の実験系を新規に立ち上げたり、原稿を書き直したり、1年がかりの改訂作業でした。
箕浦氏: 掲載された後の反響が大きかったのは、嬉しかったですね。研究会で、たくさんの方から論文について声をかけていただきました。身近な人にも多く読んでもらえたのだなと実感しました。
―― 研究の楽しさは?
武藤氏: 仮説を頭の中で組み立て、それを実験で検証したらそのとおりになった時には大きな喜びを感じます。研究室でもあれこれ考えていますが、帰宅してベッドに入ってから、突然夜中にアイデアがひらめくこともあります。脳科学の研究は、生物についての見識が深まるだけでなく、「自分」を理解することにもつながるので面白いですよね。
―― ありがとうございました。
聞き手 舘野佐保(サイエンスライター)。
【引用文献】
- Minoura, I. et al. Nature Communications 7, 10058 (2016).
- Minoura, I. et al. FEBS Letters 587, 3450-3455 (2013).
【図版】
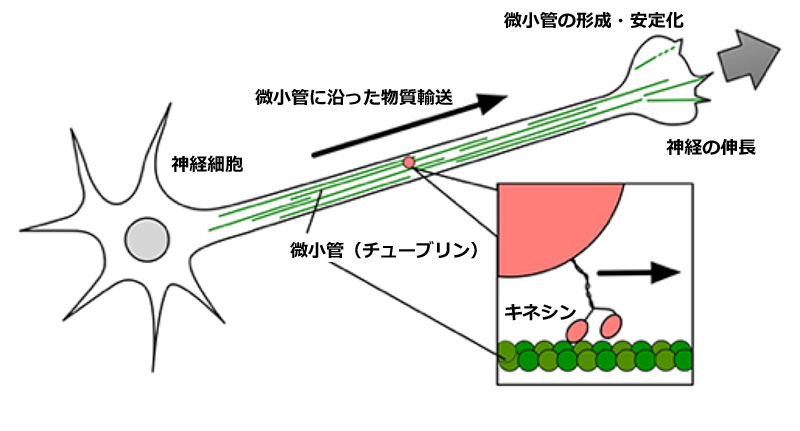
神経細胞内にはαおよびβチューブリンから形成された微小管がたくさんあり、長い神経細胞の先端へ物質を運ぶための輸送路となっている。また神経の伸長には微小管の形成が重要である。これらの働きにはモータータンパク質キネシンも重要だと考えられている。
図版出典:理化学研究所広報室
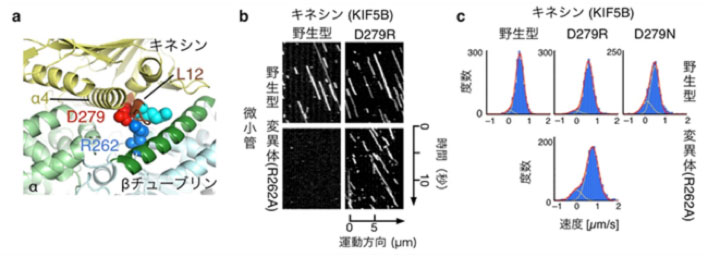
a 外眼筋繊維症の原因となるβチューブリンの変異場所の一つR262は、キネシンのL12ループと相互作用している。
b 1分子イメージングで捉えたキネシンの運動の様子を示した図。横軸が長さ方向の変位、縦軸が時間を表す。チューブリンの変異(R262A)により野生型のキネシンの運動が阻害されるが、D279R変異キネシンは変異微小管上を運動することができる。
c キネシンの運動速度も野生型とほぼ同じ程度まで回復している。
図版出典:理化学研究所広報室
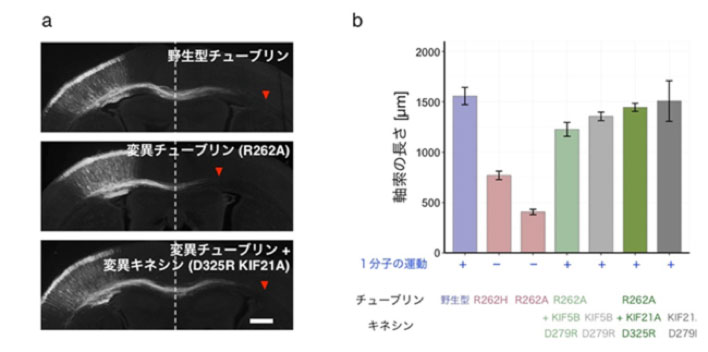
a マウス胎児の脳皮質細胞にチューブリンおよびキネシンを導入したときの脳梁の成長の差を生後3日目で観察したもの。点線が正中線、赤い三角が神経の先端。
b 正中線から神経先端までの水平長さを比較。野生型のチューブリンを導入したとき(青)と比べて、変異チューブリンを導入すると(赤)脳梁が短くなるが、変異キネシンを同時に導入すると(緑)脳梁の神経繊維の長さが回復した。
図版出典:理化学研究所広報室
Nature Communications 掲載論文
2016年1月18日掲載 Nature Communications 7 : 10058 doi:10.1038/ncomms10058
Author Profile
武藤 悦子
理化学研究所 脳科学総合研究センター
分子動態解析技術開発チーム
チームリーダー

箕浦 逸史
理化学研究所 脳科学総合研究センター
分子動態解析技術開発チーム
研究員


