Research Abstract
セプチンはHDAC6による脱アセチル化を介して微小管の安定性を負に制御することにより樹状突起と軸索の発達を促進する
セプチンはヘテロ多量体化GTP/GDP結合タンパク質のファミリーで、線虫において神経突起生成にかかわっている。上田(石原)らは、セプチンは、成長中のマウスの脳において、HDAC6を介した微小管脱アシル化を調整する足場としてこの過程を促進することを明らかにした。
Septins promote dendrite and axon development by negatively regulating microtubule stability via HDAC6-mediated deacetylation
2013年10月11日 Nature Communications 4 : 2532 doi: 10.1038/ncomms3532
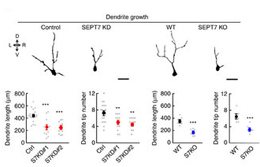
神経突起の成長には、チューブリンとセプチンという2つのGTP結合タンパク質の重合体が必要である。しかし、これらの細胞骨格系が協働しているのか、協働しているとすればどのようなメカニズムによるのかはわかっていない。本論文では、周産期マウスの大脳皮質ニューロンでセプチン重合体の必須サブユニットSEPT7をノックダウンあるいはノックアウトすると微小管が過剰にアセチル化され、大脳半球間および皮質脊髄路の軸索投射と樹状突起形成が阻害されることを示す。初代培養ニューロンを用いたin vitro実験により、SEPT7の欠乏が過剰アセチル化を介して微小管の過剰安定化ないし成長遅延をもたらすことが示された。SEPT7欠乏の表現型とα-チューブリン脱アセチル化酵素HDAC6の薬理学的阻害の表現型の類似性や両者の物理的相互作用などから、HDAC6の酵素活性ではなく、アセチル化αチューブリンとの結合にSEPT7が必要であることがわかった。以上およびその他の所見から、セプチンがHDAC6による微小管脱アセチル化の物理的足場として働くことで、微小管の安定化を神経突起成長に最適なレベルに抑制制御していることが示唆される。今回の知見により、ユビキタスに存在する2つの細胞骨格系が、神経発生過程においてはHDAC6を介して共役されていることが明らかになった。
上田(石原) 奈津実1, 宮田 卓樹2, 大島 智香1, 渡辺 雅彦3, 佐藤 良勝4, 浜村 有希4, 東山 哲也4, Ralph Mazitschek5, 尾藤 晴彦6 & 木下 専1
- 名古屋大学大学院 理学研究科 生命理学専攻 情報機構学講座 細胞制御学研究グループ
- 名古屋大学大学院 医学系研究科 機能構築医学専攻 機能形態学講座 細胞生物学分野
- 北海道大学大学院 医学研究科 解剖学講座 解剖発生学分野
- 名古屋大学 トランスフォーマティブ生命分子研究所
- Centre for Systems Biology, Massachusetts General Hospital and Harvard Medical School(米国)
- 東京大学大学院 医学系研究科 脳神経医学専攻 神経生化学分野
Neurite growth requires two guanine nucleotide-binding protein polymers of tubulins and septins. However, whether and how those cytoskeletal systems are coordinated was unknown. Here we show that the acute knockdown or knockout of the pivotal septin subunit SEPT7 from cerebrocortical neurons impairs their interhemispheric and cerebrospinal axon projections and dendritogenesis in perinatal mice, when the microtubules are severely hyperacetylated. The resulting hyperstabilization and growth retardation of microtubules are demonstrated in vitro. The phenotypic similarity between SEPT7 depletion and the pharmacological inhibition of α-tubulin deacetylase HDAC6 reveals that HDAC6 requires SEPT7 not for its enzymatic activity, but to associate with acetylated α-tubulin. These and other findings indicate that septins provide a physical scaffold for HDAC6 to achieve efficient microtubule deacetylation, thereby negatively regulating microtubule stability to an optimal level for neuritogenesis. Our findings shed light on the mechanisms underlying the HDAC6-mediated coupling of the two ubiquitous cytoskeletal systems during neural development.

