Research Abstract
ジペプチドライブラリーを用いたプロトン共役型オリゴペプチド輸送体の基質多選択性の解析
Analysing the substrate multispecificity of a proton-coupled oligopeptide transporter using a dipeptide library
2013年9月24日 Nature Communications 4 : 2502 doi: 10.1038/ncomms3502
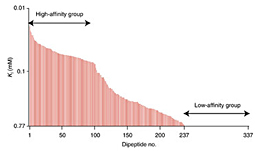
プロトン共役型のオリゴペプチド輸送体(POT)が関わるペプチド取り込みシステムは全ての生物で保存されている。POTタンパク質は特徴的な“基質多選択性”を持ち、これによって1つの輸送体が8,400種類ものジ・トリペプチド、またペプチド様医薬品を認識、輸送することができる。本論文では、ジペプチドライブラリーを用い、出芽酵母(Saccharomyces cerevisiae)の主要ペプチド輸送体であるPtr2pの基質多選択性を解析した。Ptr2pに対するジ・トリペプチドの親和性(Ki)は、48 mMから0.020 mMまで幅広く分布していることが明らかとなった。この基質多選択性は、POTファミリーメンバーが生物学的に高価値なアミノ酸の高効率な取り込みに重要な役割を担うことを示した。さらに我々は、網羅的なジペプチド群解析データと、基質分子を表現する各種物理化学的指標を用いることで、高性能の基質親和性予測モデル(正確度97%)を構築することに成功した。今回の結果は、吸収性の高いペプチドやペプチド様医薬品の開発のための重要な手掛かりを提供する。
伊藤 圭祐1,2, 疋田 礼1, 河合 駿3, Vu Thi Tuyet Lan1, 本山 貴康4, 北川 さゆり4, 吉川悠子1,2, 加藤 竜司3 & 河原崎 泰昌1,2
- 静岡県立大学大学院 薬食生命科学総合学府
- 静岡県立大学 食品栄養科学部
- 名古屋大学大学院 創薬科学研究科
- 不二製油株式会社 フードサイエンス研究所
Peptide uptake systems that involve members of the proton-coupled oligopeptide transporter (POT) family are conserved across all organisms. POT proteins have characteristic substrate multispecificity, with which one transporter can recognize as many as 8,400 types of di/tripeptides and certain peptide-like drugs. Here we characterize the substrate multispecificity of Ptr2p, a major peptide transporter of Saccharomyces cerevisiae, using a dipeptide library. The affinities (Ki) of di/tripeptides toward Ptr2p show a wide distribution range from 48 mM to 0.020 mM. This substrate multispecificity indicates that POT family members have an important role in the preferential uptake of vital amino acids. In addition, we successfully establish high performance ligand affinity prediction models (97% accuracy) using our comprehensive dipeptide screening data in conjunction with simple property indices for describing ligand molecules. Our results provide an important clue to the development of highly absorbable peptides and their derivatives including peptide-like drugs.

