内因性NLRP3インフラマソーム阻害剤であるベータヒドロキシ酪酸はストレスによって誘導される行動と炎症の応答性を減弱させる
Beta-hydroxybutyrate, an endogenic NLRP3 inflammasome inhibitor, attenuates stress-induced behavioral and inflammatory responses
2017年8月9日 Scientific Reports 7 : 7677 doi: 10.1038/s41598-017-08055-1
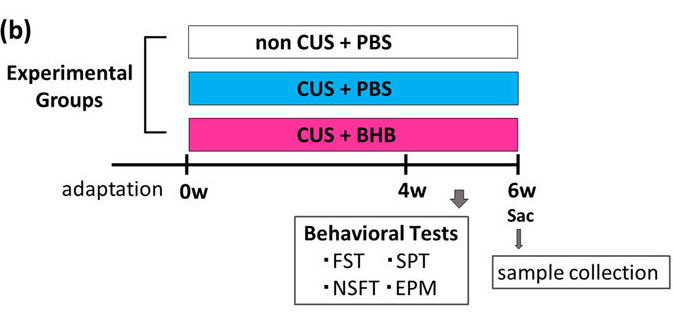
神経炎症は、うつ病の発症に非常に重要な役割を担っていることが示されている。ケトン体であるベータヒドロキシ酪酸(beta-hydroxybutyrate : BHB)は、NLRP3インフラマソームの阻害を介して抗炎症性効果を発揮することが最近報告されている。今回我々は、急性および慢性ストレスに暴露したラットにおけるBHBの抗うつおよび抗炎症効果の可能性を検討した。我々は、慢性予測不能ストレス(chronic unpredictable mild stress : CUS)によるうつ病モデル動物を用いて、抑うつおよび不安行動に対するBHBの反復投与の効果を調べた。これに加えて、拘束ストレスおよびBHB単回投与による海馬のインターロイキン-1β(interluekin-1 beta : IL-1β)および腫瘍壊死因子-α(tumor necrosis factor-alpha : TNF-α)における影響を評価した。その結果、BHBの反復投与は、CUSによって誘導される抑うつおよび不安行動を減弱した。また拘束ストレスにより海馬におけるIL-1βレベルは増加したが、BHBの事前単回投与により増加は減弱された。一方拘束ストレスによる海馬TNF-αレベルの変化は認められなかったが、BHBの単回投与によって海馬TNF-αレベルは低下した。以前我々は、ストレスによって引き起こされるIL-1βとTNF-αの放出が、NLRP3インフラマソームによって厳密に調節されることを明らかにした。これらの知見は、海馬におけるNLRP3誘導性の神経炎症を阻害することによってBHBが抗うつ様効果を発揮するであろうこと、そしてBHBがストレスに関連する気分障害の治療のための新規治療薬候補となる可能性を示している。
Corresponding Author
Neuro-inflammation has been shown to play a critical role in the development of depression. Beta-hydroxybutyrate (BHB) is a ketone body and has recently been reported to exert anti-inflammatory effects via inhibition of NLRP3 inflammasome. Here, we investigated the potential antidepressant and anti-inflammatory effects of BHB on rats exposed to acute and chronic stress. We examined the influence of repeated BHB administration on depressive and anxiety behaviors in a rodent model of chronic unpredictable stress (CUS). Additionally, the influence of acute immobilization (IMM) stress and single BHB administration on hippocampal interleukin-1β (IL-1β) and tumor necrosis factor-α (TNF-α) were assessed. Repeated administration of BHB attenuated CUS-induced depressive- and anxiety-related behaviors. IMM stress increased levels of IL-1β in the hippocampus, while a single pre-administration of BHB attenuated this increase. Although no effect was observed on hippocampal TNF-α levels after 1 h of IMM stress, a single BHB pre-administration reduced hippocampal TNF-α. Our previous report showed that the release of IL-1β and TNF-α caused by stress is tightly regulated by NLRP3 inflammasome. These findings demonstrate that BHB exerts antidepressant-like effects, possibly by inhibiting NLRP3-induced neuro-inflammation in the hippocampus, and that BHB may be a novel therapeutic candidate for the treatment of stress-related mood disorders.

