表面修飾した金ナノロッドを用いた細胞質への遺伝子導入および光熱変換による遺伝子発現誘導法
Surface chemistry for cytosolic gene delivery and photothermal transgene expression by gold nanorods
2017年7月5日 Scientific Reports 7 : 4694 doi: 10.1038/s41598-017-04912-1
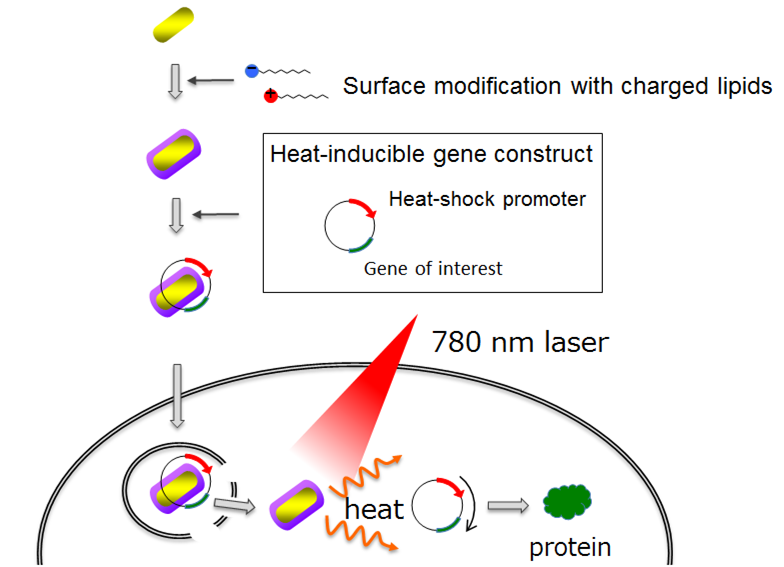
遺伝子発現の光操作技術は、標的細胞の運命や機能を遠方から非侵襲的に制御する方法として大きな可能性をもたらす。このような制御を達成する1つの方法に、熱ショックタンパク質(HSP)プロモーター駆動型タンパク質発現ベクターと光熱変換ヒーターを細胞内に導入し、光照射による活性化を行う方法がある。本研究では、金ナノロッド(AuNR)をオレイン酸およびDOTAP(1,2-dioleoyl-3-trimethlammonium-propane)という2つのありふれた脂質を用いて機能化することで、細胞への効率的な遺伝子導入やHSPプロモーターの迅速な光活性化が可能であることを示す。我々のAuNR(DOTAP-AuNR)を用いる方法は、細胞への遺伝子導入効率の点で、リポフェクタミン2000を用いる方法に匹敵し、さらに細胞毒性はより低かった。次に、DOTAP-AuNRで遺伝子導入した細胞に10秒間、近赤外レーザー(NIR)照射を行うと、有意な光毒性を示すことなく、照射時間と部位に特異的に導入遺伝子の発現が誘導された。この効率は培養皿全体を42°Cで30分間加熱した場合と同程度であった。このメカニズムを調べたところ、効率的な遺伝子導入とHSPプロモーター(HSP70b’)の迅速な光活性化は、DOTAP-AuNRのエンドソーム脱出が促進されているためであると考えられた。我々は、遺伝子導入と光線温熱加熱にそれぞれ独立して用いられてきたありふれた3つの成分を適切に組み合わせることで、NIR照射部位特異的な遺伝子発現のための新しいプロトコルが開発できることを示す。
Corresponding Author
Light-inducible gene regulation has great potential for remote and noninvasive control of the fate and function of target cells. One method to achieve such control is delivery of heat shock protein (HSP) promoter-driven protein expression vectors and photothermal heaters into the cells, followed by activation by illumination. In this study, we show that gold nanorods (AuNRs) functionalized with two conventional lipids, oleate and 1,2-dioleoyl-3-trimethylammonium-propane (DOTAP), are capable of efficient transfection and quick photoactivation of the HSP promoter. Use of our AuNRs (DOTAP-AuNRs) was comparable to Lipofectamine 2000 in terms of transfection efficiency, while lower in cytotoxicity. Subsequent near-infrared laser (NIR) illumination of the cells transfected by DOTAP-AuNRs for 10 s induced time- and site-specific transgene expression without significant phototoxicity, to a degree similar to that of heating the entire culture dish for 30 min. Our mechanistic studies suggest that efficient transfection and quick photoactivation of the HSP promoter (HSP70b’) are due to the promoted endosomal escape of DOTAP-AuNRs. We propose a novel protocol for NIR-inducible, site-directed gene expression using an unprecedented complex of the three conventional components capable of both transfection and photothermal heating.

