新規インドール化合物MA-35はTNF-αおよびTGF-β1経路の両方を阻害することにより腎臓線維化を軽減する
A novel indole compound MA-35 attenuates renal fibrosis by inhibiting both TNF-α and TGF-β1 pathways
2017年5月15日 Scientific Reports 7 : 1884 doi: 10.1038/s41598-017-01702-7
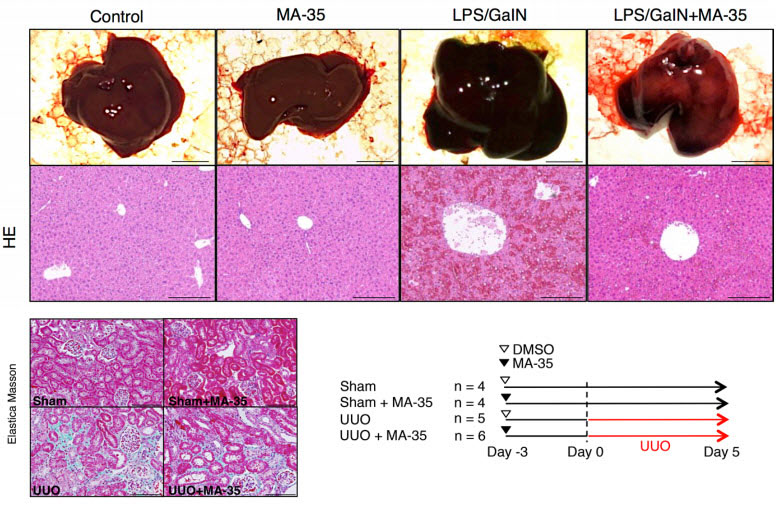
腎臓の線維化は慢性炎症と深く関わりがあり、エピジェネティクス機構にも制御されている。トランスフォーミング増殖因子-β1(TGF-β1)および腫瘍壊死因子-α(TNF-α)のシグナル伝達は、腎臓線維化の進行に重要な役割を果たしているので、その治療法としてTGF-β1とTNF-αの両方の阻害が望ましい。今回我々は、インドール誘導体の化合物ライブラリーにおいて、抗TNF-α作用を示す低分子化合物をスクリーニングした。41種類のインドール誘導体のうち11種類がTNF-αの作用を阻害した。それらの中で、5-(3,5-ジメトキシベンジルオキシ)-3-インドール酢酸であるMA-35(Mitochonic Acid-35)は、最も強力な作用を示した。MA-35はIBキナーゼのリン酸を阻害することによって抗TNF-α作用を示し、マウスにおいてLPS-GalNにより誘導される肝臓の炎症を軽減した。さらにMA-35はSmad3のリン酸化を阻害することによって抗TGF-β1作用を示し、TGF-β1により誘導される線維化遺伝子の発現を抑制した。腎臓線維化モデルである片側の尿管を結紮したマウスの腎臓において、MA-35は炎症性サイトカインと線維化遺伝子の発現を抑制し腎臓の炎症と線維化を軽減した。さらにMA-35はTGF-β1により誘導される線維化遺伝子のプロモーター領域のヒストン修飾H3K4me1を阻害し、線維化遺伝子の発現を抑制した。MA-35は線維化に関与する複数のシグナル伝達経路に影響を与え、さらにエピジェネティック修飾を回復させると考えられる。したがってMA-35は線維症に対する新規治療薬となる可能性がある。

