遺伝子コード型のシステムで生体内のヒストン修飾を追跡する
Genetically encoded system to track histone modification in vivo
2013年8月14日 Scientific Reports 3 : 2436 doi: 10.1038/srep02436
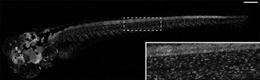
ヒストンの翻訳後修飾は、遺伝子制御や発生、分化において主要な役割を担っているが、生体内におけるその動態は、全くといっていいほど分かっていない。この問題に取り組むために、我々は生体内でヒストン修飾を追跡することのできる修飾特異的細胞内抗体プローブ(mintbody;modification-specific intracellular antibody)の発現系を開発した。H3リシン9のアセチル化特異的mintbody(H3K9ac-mintbody)を作製し、ヒトの細胞に安定的に発現させたところ、H3K9ac-mintbodyの細胞核内における局在は、標的となるアセチル化の局在とよく一致し、ユークロマチン領域への濃縮が見られた。また、H3K9ac-mintbodyの動態変化を利用して、ヒストン脱アセチル化酵素阻害剤処理によるアセチル化量の変動を、生細胞内で測定することができた。我々はさらに生体内のヒストン修飾を追跡するために、H3K9ac-mintbodyを発現するショウジョウバエとゼブラフィッシュのトランスジェニック系統を作製した。ショウジョウバエ(Drosophila)の胚発生では、H3K9ac-mintbodyの局在は劇的に変化し、第7分裂周期辺りの胚性遺伝子活性化に伴うアセチル化の上昇を明らかにすることができた。以上のように、本研究はmintbodyの多岐にわたる可能性を示しており、生体内でのエピジェネティック解析の基礎となるものである。
佐藤 優子1,2, 向 正則3, 上田 潤4, 村木 倫子5, Timothy J. Stasevich1, 堀越 直樹6, 鯨井 智也6, 北 大晃3, 木村 泰介3, 平 誠司3, 岡田 康志7, 林-高中 陽子1,2, 小布施 力史8, 胡桃坂 仁志6, 川原 敦雄5, 山縣 一夫4, 野崎 直仁9 & 木村 宏1,2
- 大阪大学大学院 生命機能研究科
- JST-CREST
- 甲南大学 理工学部 生物学科
- 大阪大学 微生物病研究所
- 理化学研究所 QBiC循環器分子動態研究ユニット
- 早稲田大学 理工学術院
- 理化学研究所QBiC細胞極性統御研究チーム
- 北海道大学大学院 先端生命科学研究院
- 株式会社モノクローナル抗体研究所

