システイン tRNA 合成酵素はシステインポリスルフィド生成とミトコンドリアのエネルギー産生をコントロールしている
Cysteinyl-tRNA synthetase governs cysteine polysulfidation and mitochondrial bioenergetics
2017年10月27日 Nature Communications 8 : 1177 doi: 10.1038/s41467-017-01311-y
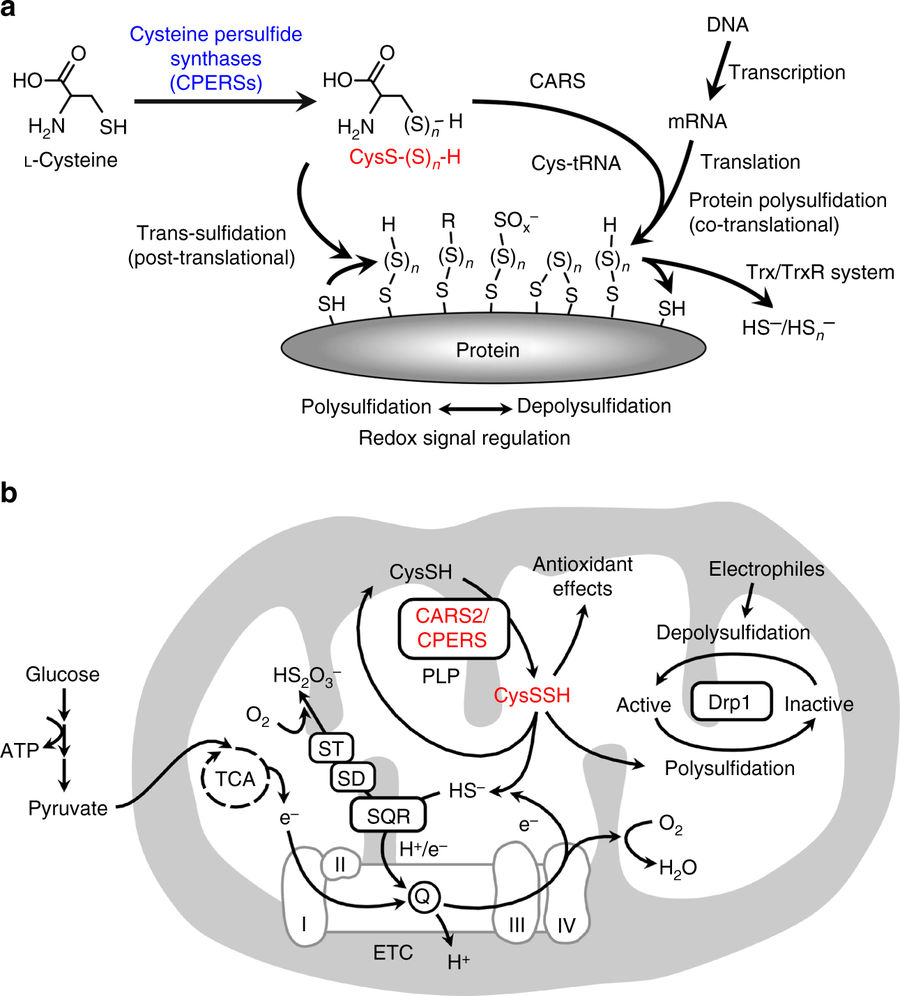
システイン(CysSH)のチオール基にイオウ原子が過剰に挿入されたシステインパースルフィド(CysSSH)は様々な生物種で豊富に存在しているが、その生合成および生理学的機能についてはほとんど知られていない。今回我々は、原核生物および哺乳類のシステインtRNA合成酵素(CARS)が、CysSHを基質としてCysSSHを合成することを発見した。そして、大腸菌や哺乳類細胞のシステイン含有タンパク質にCysSSHが非常に多く含まれることを見出し、CARSにより合成されるCysSSHがタンパク質の翻訳時に直接ポリペプチドに取り込まれることを明らかにした。さらに、マウスおよびヒト細胞のミトコンドリア型CARS (CARS2)をノックアウトすると、組織・細胞中のCysSSHのレベルが顕著に低下し、この酵素がin vivoで主要なシステインパースルフィド合成酵素として機能いることが証明された。さらに、細胞のCysSSHのレベル低下により、ミトコンドリアの断片化・膜電位形成不全、酸素消費の抑制がみられた。こうしたミトコンドリアの異常は、CARS2のCysSSH合成活性の回復により消失することから、ミトコンドリアにおけるCysSSH生成がミトコンドリアの形態形成およびエネルギー代謝や呼吸機能の発現・維持に必須であるといえる。したがって、今回のCARS依存的パースルフィド産生メカニズムの発見が、生理学的および病態生理学的なレドックスシグナル制御機構の解明や、酸化ストレスおよびミトコンドリア機能障害に基づく治療標的の探索に大きく貢献することが期待される。
Corresponding Author
Cysteine hydropersulfide (CysSSH) occurs in abundant quantities in various organisms, yet little is known about its biosynthesis and physiological functions. Extensive persulfide formation is apparent in cysteine-containing proteins in Escherichia coli and mammalian cells and is believed to result from post-translational processes involving hydrogen sulfide-related chemistry. Here we demonstrate effective CysSSH synthesis from the substrate L-cysteine, a reaction catalyzed by prokaryotic and mammalian cysteinyl-tRNA synthetases (CARSs). Targeted disruption of the genes encoding mitochondrial CARSs in mice and human cells shows that CARSs have a crucial role in endogenous CysSSH production and suggests that these enzymes serve as the principal cysteine persulfide synthases in vivo. CARSs also catalyze co-translational cysteine polysulfidation and are involved in the regulation of mitochondrial biogenesis and bioenergetics. Investigating CARS-dependent persulfide production may thus clarify aberrant redox signaling in physiological and pathophysiological conditions, and suggest therapeutic targets based on oxidative stress and mitochondrial dysfunction.

