腸粘膜が分泌する、悪玉菌を一括して抑えるIgA抗体を発見!
新藏 礼子、岡井 晋作、臼井 文人
2016年6月号掲載
ヒトの腸内には、最大で数千種類、1000兆個にも及ぶ腸内細菌が住み着いているという。菌の種類や数は食生活や健康状態によって大きく変わるとされ、腸内細菌叢がさまざまな疾患に関与していることもわかってきた。奈良先端科学技術大学院大学(NAIST)の新藏礼子教授らは、腸粘膜で分泌されるIgA抗体を1種ずつ分離し、その一つに腸内細菌に幅広く結合し、増殖を抑える機能があることを突き止めた。
―― 長浜バイオ大からともにNAISTに移られたのですね。
岡井氏: 私も臼井君も長浜バイオ大に入学し、3年次に新藏先生の研究室に入りました。私の方が1年上級で、研究室の一期生でもあります。ともに、そのまま修士、博士課程へと進みましたが、この4月に先生がNAISTへ移られるのを機に、私たちもこちらに編入してきました。
新藏氏: 京都大学大学院医学研究科で准教授だったときに、「独立できたら、腸管粘膜から分泌されるIgAをモノクローナルに分離して腸内免疫について解明したい」と思っていました。2010年に長浜バイオ大で研究室を持つことになり、マウスを対象に、IgAが腸内細菌叢の制御にどのように関与しているのかを明らかにしようと考えました。研究室の立ち上げとともに岡井君が入ってきましたので、彼とともにまず「IgAを産生させるための細胞(ハイブリドーマ)作り」を始め、それが今回の成果に至る原点となりました。紆余曲折はありましたが、論文はこの7月刊行のNature Microbiology で発表することができました。実験の大半はほぼ長浜バイオ大でなされたものですが、私はこの4月にNAISTに着任し、同時に2人もこちらに編入して現在に至っています。
W27抗体の単離と腸内細菌の認識機構
―― どのようにしてIgAを単離したのでしょう?
岡井氏: まず、野生型マウスの小腸粘膜でIgA産生するB細胞を採取し、多発性骨髄腫(ミエローマ)細胞と融合させて不死化させました。それらの個々の細胞を培養して増やし、IgA 抗体を作らせました。200種以上のIgA 産生ハイブリドーマを作製しましたが、最終的に16種をリストアップしました。
―― 得られたIgAは腸内細菌と反応させたのですか?
新藏氏: はい。かねてより私は、腸内ではたらくIgAの中には多種類の細菌に作用して増殖を抑えるものがあるのではないかと考えていました。そこで、俗に善玉といわれるカゼイ菌やビフィズス菌、悪玉といわれる大腸菌、サルモネラ菌などの約20種を対象に、リストアップした16種のIgAと反応させてみました。私の予想は大当たりで、W27となづけたただ一つの抗体が際立って多種類の細菌と反応し、高いレベルで結合することがわかりました。
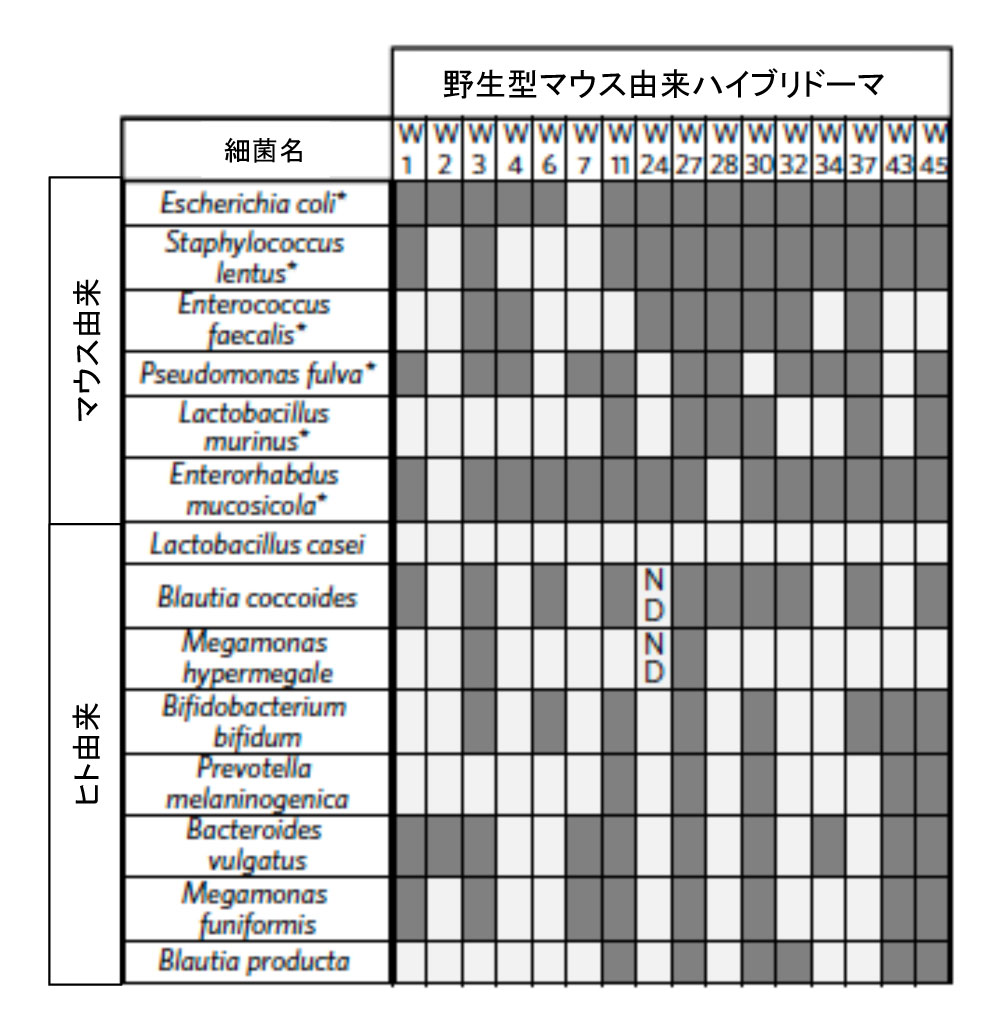
全IgA 抗体が、少なくとも3種の異なる腸内細菌に結合した。グレー:結合する、白:結合しない、ND:未検討。 | 拡大する
それまでの私たちは、腸内細菌のような嫌気性の細菌を扱ったことがなかったので、ここでヤクルト中央研究所に協力いただいて培養方法を教わったり、細菌サンプルを分けていただいたりしました。一部には、私たちがマウスの便から独自に採取して培養した細菌もあります。
翌年、臼井君が入ってきましたので、彼には、W27が細菌のどういう部分を認識して結合するのかを調べてもらうことにしました。
―― 具体的にどのようにされたのでしょう?
臼井氏: まず、大腸菌などの数種の細菌のタンパク質を抽出し、W27抗体が認識する分子をウエスタン解析で可視化しました。その結果、W27抗体が認識する分子は約50キロダルトンであることがわかりました。
次に、このタンパク質のアミノ酸配列を割り出し、データベースを使ってどのようなタンパク質なのかを検索してみました。当然、細菌の膜上でW27抗体と結合しているものと考え、膜タンパク質に分類されるものがヒットしてくるだろうと予想したのですが、そのようなものはありませんでした。かわりに、なぜだかSHMT(セリン・ヒドロキシメチル・トランスフェラーゼ)という代謝酵素がヒットしてきました。はじめは何かの間違いだろうと思って無視していたのですが、何度やり直しても出てくるので、SMHTについて調べてみると、この酵素が細菌の外膜と内膜の間に存在するタンパク質であることがわかりました。
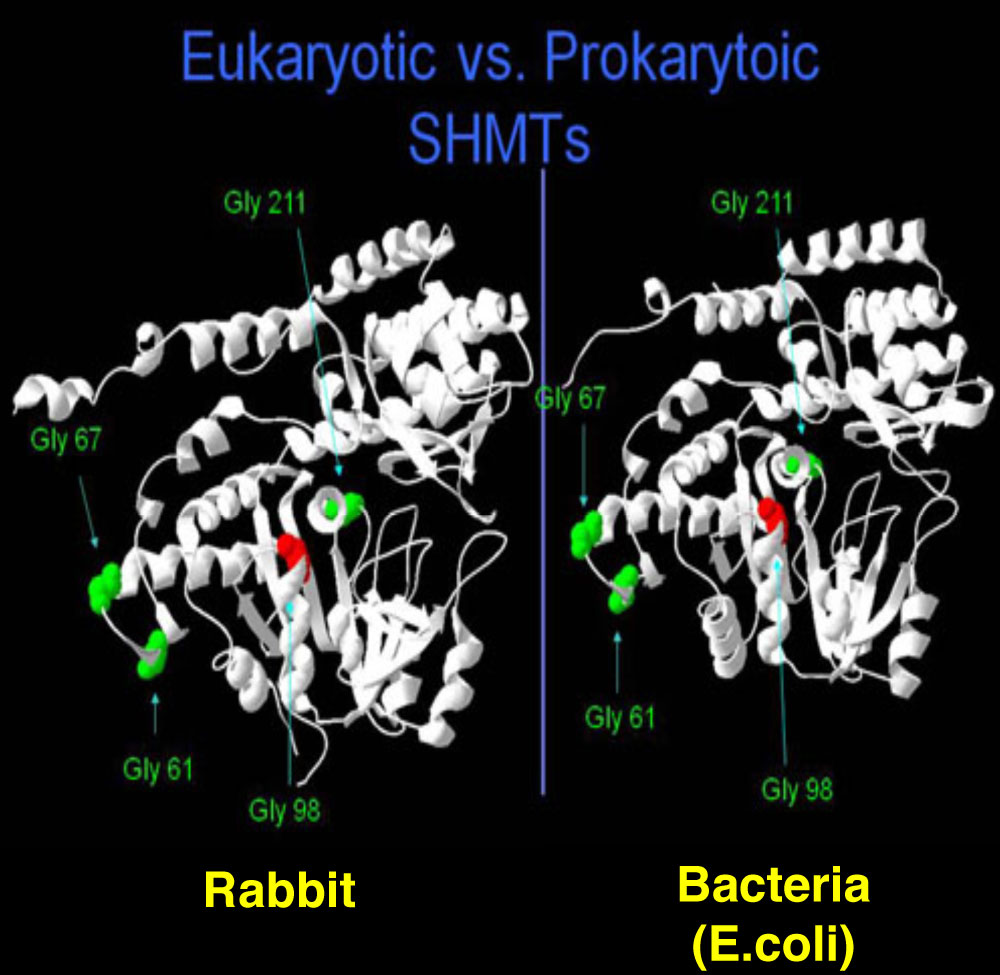
SHMTの分子構造は、大腸菌から哺乳動物まで良く保存されている。大腸菌では二量体で、哺乳動物では4量体として機能する。 | 拡大する
―― 認識する相手はSMHTだったのですか?
臼井氏: はい、そう結論付けました。よく調べてみると、SHMTは細菌からヒトにいたる生物に共通して保存されているタンパク質で、葉酸代謝に関与する酵素として知られ、DNA合成やアミノ酸代謝に関わるものでした。そこで考えを改め、W27抗体が病原性細菌のSMHTに結合することで、細菌のDNA合成や細胞分裂が抑制されるのではないかと解釈しなおしました。
次に、大腸菌などのSMHT のアミノ酸配列を、W27抗体と結合しないカゼイ菌、マウス、ヒトなどの配列と比較し、W27抗体がどこをエピトープとして認識しているのかを調べ、「ある特定部分の4アミノ酸」であることを突き止めました。病原性細菌として知られる細菌の多くでは、SMHTの4アミノ酸の配列が「EEHI」となっていましたが、善玉菌として知られる細菌や哺乳類のSMHTでは全く異なっており、W27抗体が認識できないとわかりました。想像の域を出ませんが、細菌のSMHTは構造的に一部が外膜の外に出ていて、W27抗体が認識可能なのではないかと考えています。
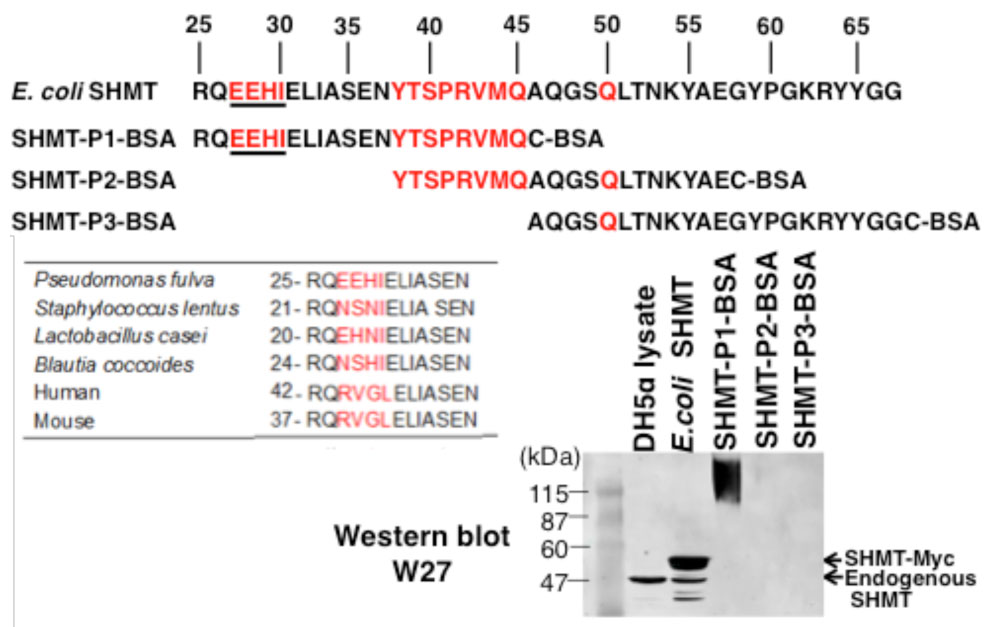
W27抗体は、大腸菌のSHMT のN 末アミノ酸配列25-45番目のペプチド(SHMT-P1-BSA)に特異的に反応した。この配列内には赤字で示した「種によって異なる4アミノ酸配列」が存在し、W27抗体はこの配列の違いを識別することで細菌を選別すると考えられる。 | 拡大する
増殖抑制効果を個体レベルで検証
―― 次は生体マウスで検証されたわけですね。
新藏氏: 「抗原との結合力が弱いIgAしか作れない遺伝子変異体マウス(AIDG23Sマウス)」を正常マウスと比較することで、腸管でIgAを産生するB細胞の活性化と腸内細菌叢との関係を調べてみました。AIDG23Sマウスは、長浜バイオ大のさらに前職の京大時代に、私も開発に携わることで得られたものです1。
まず、AIDG23マウスの腸内細菌叢は悪玉とされる細菌が多く、B細胞が過剰に活性化された状態にあることがわかりました。このB細胞はIgAを作っているものの、質が悪いために悪玉細菌を駆逐できず、結果として細菌叢のバランスが崩れていると解釈できました。このようなマウスは、腸粘膜の免疫系が過剰活性化されて腸粘膜損傷が生じており、見た目にも毛並みがよくありませんでした。
岡井氏: 次に、これらの2種のマウスに、飲料水にW27抗体を混ぜて好きなだけ飲ませてみました。生後10〜17週令の、ヒトでいうと中年くらいを対象にしました。投与4週間後に便と腸粘膜組織を詳しく調べてみたところ、AIDG23Sマウスでは、B細胞の過剰な活性化が鎮まり、腸内細菌のバランスが正常に近づいて、腸粘膜組織の異常も改善されていました。見た目にも毛並みがよくなりました。経口投与したW27抗体が腸管ではたらき、悪玉細菌の増殖を抑えた結果だと解釈できます。そして、2次的に善玉菌が増えたのだと思われます。正常マウスの方は、とくに変化はみられませんでした。
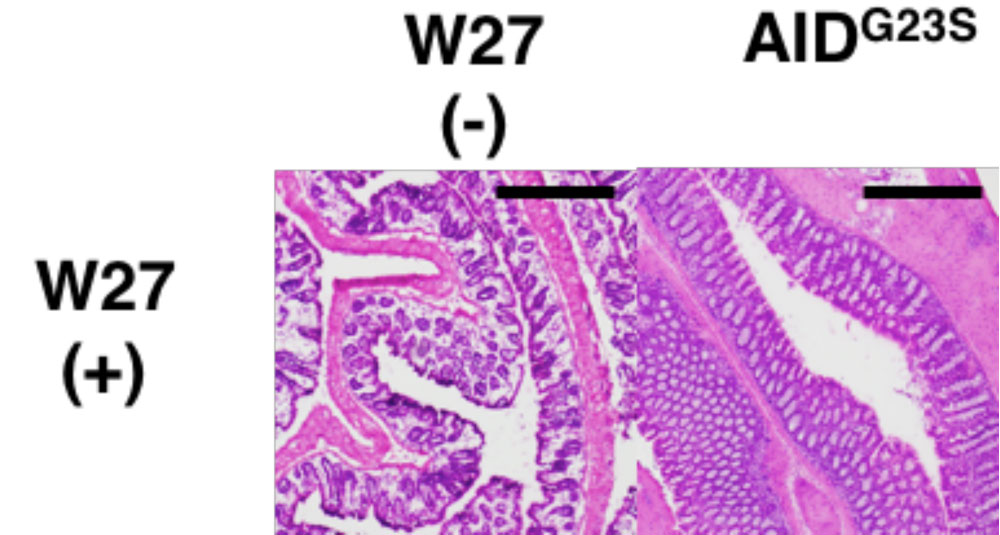
投与前の大腸の損傷(クリプト数の減少)が見られたが、抗体投与後には改善された。 | 拡大する
―― W27抗体は経口投与でも機能を維持するのですか?
新藏氏: はよくそのような質問を受けるのですが、母親のIgA抗体が母乳を通して新生児の腸に移行することはよく知られており、抗体が胃酸ですべて分解されることはないと思います。検証のために、腸管IgA抗体を全くもたないマウス(AIDノックアウトマウス)にW27抗体を投与し、その後で腸粘膜組織を切り出して調べ、飲んだW27抗体がきちんと腸全体に分布していることも確かめました。
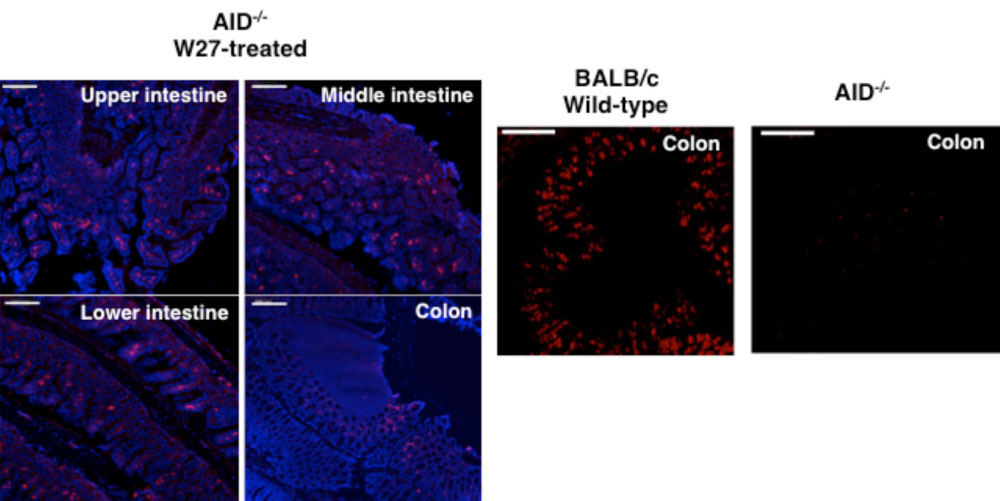
IgA抗体を産生しないAIDノックアウトマウスにW27抗体を経口投与した。その後、マウスを解剖して各部の腸の組織切片を抗IgA抗体で染色し、経口投与されたW27抗体が腸管全長に分布することを確認した。 | 拡大する
論文にまとめる苦労と今後について
―― さまざまな病気の治療薬開発に応用できそうな成果ですね。
新藏氏: まさに、そこを狙っています。さまざまな先行研究により、腸内細菌の一部が生体に異常な刺激を与えることで生体システムがみだされ、さまざまな病気につながると考えられるようになっています。たとえば、潰瘍性大腸炎、クローン病などの炎症性腸疾患や、アレルギー、自己免疫疾患、がん、糖尿病、ある種の精神神経疾患などです。私たちは、今回のW27抗体を薬として使うことで、このような患者さんの腸内細菌叢を改善する薬が開発できるとよいと考えています。そのために次のステップとして、患者さん由来の便をマウスに移植し、マウス腸内においてヒト腸内細菌に対するW27抗体の効き目を検証したいと計画しています。一方で、家畜に投与することで、濫用が問題視されている抗生物質の量を減らせるのではないかなどとも考えています。
―― Nature Microbiology とのリバイスはどのようでしたか?
新藏氏: 実は、はじめはNature に投稿したのですが、データが不足していると判断されてうまくいきませんでした。そこで並行して何誌かに投稿しなおしましたが、幸運なことに新たに創刊されるNature Microbiology が受け入れてくださり掲載が叶いました。いくつか追加実験なども指示されましたが、不要な実験は率直に反論し、ご理解いただくこともできました。参考になる論文など、ありがたいご教示もありました。投稿から掲載までは比較的順調だったと思います。
前述のヤクルト中央研究所の松本敏先生のグループ、理化学研究所の大野博司先生のグループ、そして国立遺伝学研究所(元東京工業大学)の黒川顕先生のグループ、そのほか多くの共同研究者のご協力なくしては、論文を仕上げるのは無理だったと思います。みなさんへの感謝とともに、研究者のネットワークを構築することの重要性も痛感しました。
―― 岡井さんにとっては学位論文になったと伺いました。
岡井氏: はい、おかげさまで無事卒業できそうです。卒業後も腸内免疫の領域にいたいと考えていますが、どこでどのようなことをするかはまだ決めかねています。
臼井氏: 治療困難な腸炎の原因菌であるClostridium difficile菌、糖尿病との関連が示唆されるPrevotella菌などを対象にW27抗体との反応について解析を進め、卒業論文を書き始めたいと考えているところです。
新藏氏: 岡井君は実によく実験をこなす学生です。私の研究室内で最も多くの注文を突きつけた学生だと思いますが、よくやってくれました。臼井君はじっくり考えるタイプで、私はなるべく邪魔をしないようにしています。
現在は9人の学生がいますが、2人は後輩をよく指導してくれています。私自身は研究資金の獲得などに苦戦していますが、企業との共同研究やW27抗体を飲ませてみたいとおっしゃってくださる先生方とともに、W27抗体の薬剤利用に向けた研究を続けたいと考えています。
―― ありがとうございました。
聞き手は、西村尚子(サイエンスライター)。
引用論文
- Wei et al., Nat. Immunol., 12, 264-270, 2011
Nature Microbiology 掲載論文
Article: 高親和性モノクローナルIgAはマウスの腸内微生物相を調節し、大腸炎を防止する
High-affinity monoclonal IgA regulates gut microbiota and prevents colitis in mice
Nature Microbiology 1 : 16103 doi:10.1038/nmicrobiol.2016.103 | Published online 04 July 2016
Author Profile
新藏 礼子(しんくら れいこ)
京都大学医学部卒業後、麻酔科医として勤務。京都大学大学院医学研究科で医学博士を取得。大学院で抗体の研究に出会う。その後、ハーバード大学留学、京都大学大学院医学研究科免疫ゲノム医学准教授、長浜バイオ大学バイオサイエンス学科教授を経て、2016年4月より奈良先端科学技術大学院大学バイオサイエンス研究科教授。大学院時代から抗体遺伝子の組換えの研究を継続している。

岡井 晋作(おかい しんさく)
2012年、長浜バイオ大学卒業。2014年、長浜バイオ大学大学院前期課程修了。2016年、奈良先端科学技術大学院大学後期課程在学(新藏礼子教授)。腸管IgA抗体による腸内細菌制御機序の解明の研究を行っている。

臼井 文人(うすい ふみひと)
2013年、長浜バイオ大学卒業。2015年、長浜バイオ大学大学院前期課程修了。2016年、奈良先端科学技術大学院大学後期課程在学(新藏礼子教授)。腸管IgA抗体が認識する腸内細菌分子の解明の研究を行っている。



