肝臓でのアミノ酸/mTOR/S6K依存的シグナル伝達経路は神経シグナルを介して全身での脂質代謝を調節する
A hepatic amino acid/mTOR/S6K-dependent signalling pathway modulates systemic lipid metabolism via neuronal signals
2015年8月13日 Nature Communications 6 : 7940 doi: 10.1038/ncomms8940
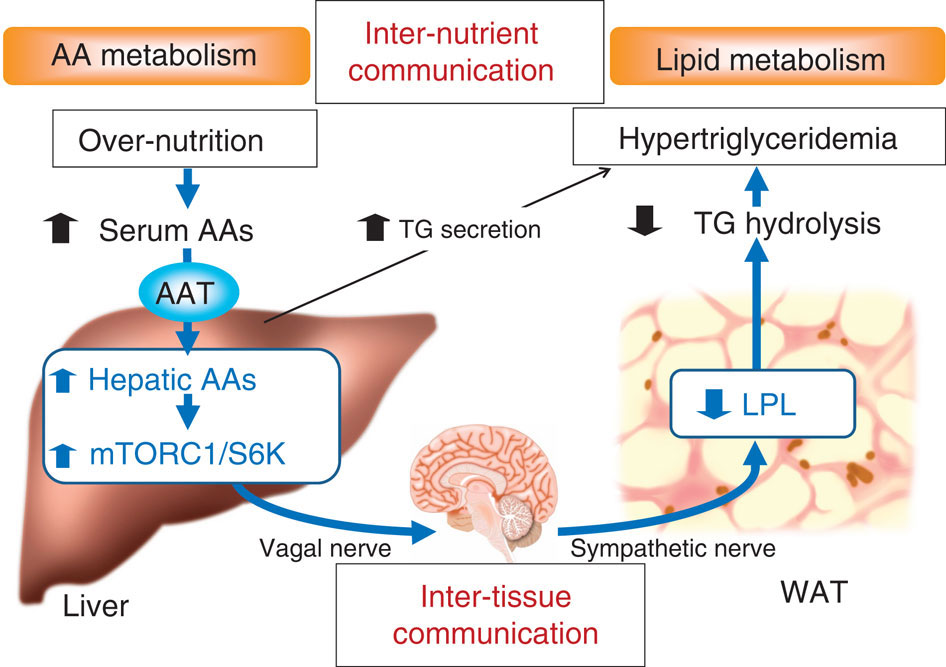
栄養素代謝は神経シグナルを介する組織や臓器の連携により、個体レベルで調整されている。血中のアミノ酸(AA)レベルは肥満状態では上昇しており、肝臓で細胞内のmTORC1(mammalian target of rapamycin complex-1)/S6キナーゼ(S6K)経路を活性化していることが知られている。今回我々は、肝臓でのAA/mTORC1/S6K経路の活性化が、神経シグナルによる組織間の情報伝達機構を介して、全身での脂質代謝を調節することを実証した。AAトランスポーターであるSNAT2を肝臓で発現させると、肝でのmTORC1/S6K経路が活性化した。その結果、脂肪組織でのリポタンパクリパーゼ(LPL)の発現低下をともない、血清のトリグリセリド(TG)が顕著に上昇した。肝臓でRhebあるいは活性型S6Kを発現させても同様の代謝効果が認められ、肝臓でドミナントネガティブS6Kを発現させることではSNAT2マウスの血中TG上昇を抑制したことから、AA/mTORC1/S6K経路の活性化の関与が示された。肝迷走神経切断や薬理学的求心路遮断およびβブロッカー投与を行うとこれらの代謝効果は消失し、肥満マウスでも脂肪組織でのLPL発現が上昇し高トリグリセリド血症が抑制されたことから、求心性迷走神経と遠心性交感神経から成る神経経路がこの肝臓と脂肪組織の間の代謝情報伝達に関わっていると考えられる。以上から、今回解明された神経機構はアミノ酸と脂質といった栄養素間の代謝連携に役立つとともに、肥満の際に生ずる高トリグリセリド血症の発症にも寄与していることが明らかとなった。
Kenji Uno, Tetsuya Yamada, Yasushi Ishigaki, Junta Imai, Yutaka Hasegawa, Shojiro Sawada, Keizo Kaneko, Hiraku Ono, Tomoichiro Asano, Yoshitomo Oka & Hideki Katagiri

