子宮筋腫
Uterine fibroids
2016年6月23日 Nature Reviews Disease Primers Article number: 16043 (2016) doi: 10.1038/nrdp.2016.43
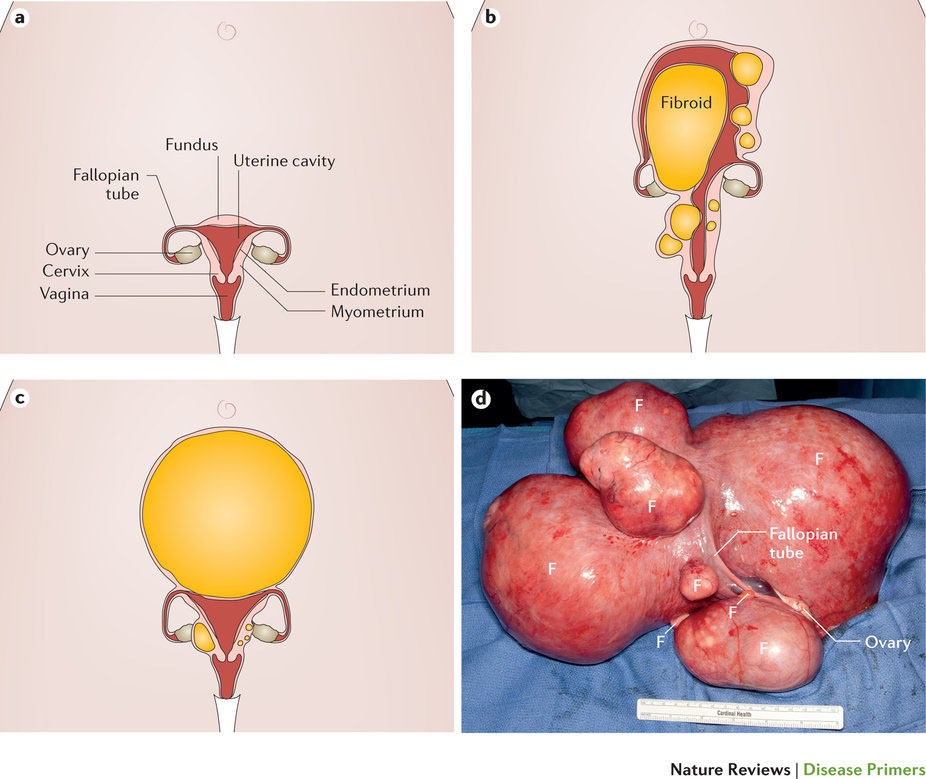
子宮筋腫(uterine fibroids、別名:leiomyomasまたはmyomas)はよく見られる子宮のクローン性の腫瘍である。筋腫は線維性細胞外マトリックスに加えて平滑筋と線維芽細胞の両方から成り、これらいずれの成分も発症過程に寄与する。筋腫の病態生理、大きさ、局在および臨床症状は極めて多様である。筋腫には悪性化する変異体も若干あるが概して良性であり、このことも疾患範囲の一部になっている。筋腫のリスクと人種には関連がある。若年黒人女性の筋腫の発症リスクは、同年代の白人女性と比べて高いことに加え、より重症化して発症する。臨床的には、すべての子宮摘出術例の1/3から1/2の原因が筋腫であり、妊娠適齢期の女性における高い罹患率と高額な医療費に関連している。実際、現在の治療は外科手術とインターベンション療法が中心になる。筋腫治療の約3/4は子宮摘出術が占めている。しかし、プロゲステロン受容体修飾薬による薬物治療によって、臨床に革新がもたらされている。筋腫形成の原因となる遺伝的サブグループに関する新たな情報が急速に蓄積されることで、子宮筋腫の臨床的多様性の理解が深まり、個別化治療につながることが期待される。このような情報は、治療の意思決定の基礎となる高品質なエビデンスが不十分な現状にとって重要な進歩といえる。
PrimeView
子宮筋腫はよく見られる子宮の腫瘍で、疼痛および泌尿器系や消化器系の問題をはじめ、重度または長期の月経出血の原因となる。このPrimeViewでは子宮筋腫の発症機構を中心に取りまとめる。
本Primerの図解サマリー

