طفرة في عالم الجراحة: آلية للتحايل على رفض الجسم البشري لأعضاء الخنازير
26 November 2025
نشرت بتاريخ 26 نوفمبر 2025
يمكن، عبر إدخال تعديلات جينية على الأعضاء المأخوذة من الخنازير، منع الجهاز المناعي البشري من مهاجمتها عند زرعها في جسم الإنسان.
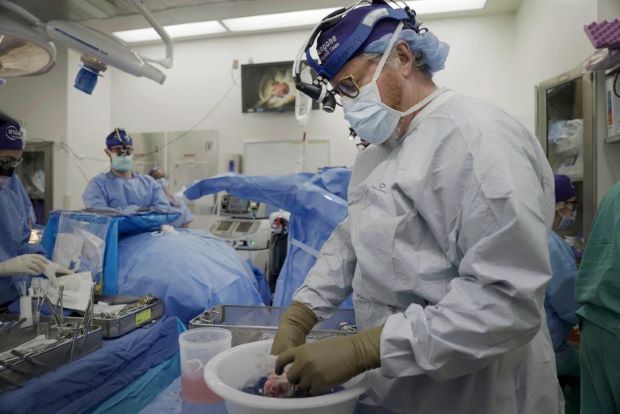
في الولايات المتحدة، نجح مؤخرًا فريق من العلماء في الحيلولة دون رفض جسم رجل - بلغ من العمر 57 عامًا وأعلنت وفاته دماغيًا – لكلية خنزير. وبعد الجراحة، أمكن للكُلية أن تؤدي وظائفها داخل جسد الرجل لـ61 يومًا، في ما يُعد أطول مدة استمرت خلالها وظائف عضو خنزير معدل جينيًا في شخص ميت دماغيًا.
في هذا الإطار، في دراستين 1، 2 نشرتا مؤخرًا في الثالث عشر من نوفمبر الجاري في دورية Nature، وصف باحثون العوامل الأساسية التي تسبب رفض الجهاز المناعي بالجسم البشري للأعضاء المستزرعة في الإنسان. ونتائج الدراستين - بحسب باحثين - من شأنها أن تحسن نتائج جراحات استزراع الأعضاء المأخوذة من أشخاص آخرين أو من الحيوانات.
وعن هذه النتائج، يقول محمد محيي الدين، الباحث الإكلينيكي في كلية الطب بجامعة ميريلاند في مدينة بالتيمور الأمريكية، والذي أشرف على أول جراحة زرع قلب خنزير في جسد شخص حي عام 2022: "أعتقد أنها الأولى في إرشادنا إلى كيفية منع الرفض المناعي".
يشار إلى أنه خلال الأعوام الثلاثة الماضية، تلقى عشرات الأشخاص خلال حيواتهم أعضاء مأخوذة من خنازير معدلة جينيًا، كالقلب، أو الكُلية أو الكبد أو الغدة الصعترية. غير أن غالبية هذه الأعضاء استُأصلت في نهاية المطاف، بعد أن توقفت عن أداء وظائفها أو بعدما لم تعد ذات جدوى كافية تبرر الاستمرار في إعطاء العلاج الكابت للمناعة المطلوب. وبعض متلقيي هذه الأعضاء توفوا بعد وقت قصير من جراحة الاستزراع.
وفي جراحة استزراع كُلية الخنزير سالفة الذكر، تلقى الرجل الذي نقلت له الكلية أيضًا غدة صعترية، وهي غدة صغيرة تُدرِب الجهاز المناعي على التمييز بين الأنسجة الدخيلة على الجسم والخلايا الخاصة به. ويرجح أن الغدة الصعترية لعبت دورًا كبيرًا في نجاة كُلية الخنزير لوقت أطول من هجمات الجهاز المناعي في جسم متلقيها، بحسب ما يفيد روبرت مونتجومري، المؤلف المشارك في الدراسة التي أسفرت عن الجراحة، وهو جراح وباحث في «معهد لانجون لزراعة الأعضاء بجامعة نيويورك» في مدينة نيويورك الأمريكية. ففي التجارب السابقة التي أُجريت على رئيسيات من غير البشر، نجت الكُلية المُعدلة جينيًا بدرجة أكبر من هجمات الجهاز المناعي عندما استزرعت مع الغدة الصعترية، مقارنة بها عندما استزرعت دون الغدة.
كيف يمكن تلافي رفض الأعضاء المستزرعة؟
أُجريت جراحة زرع الكُلية في الرابع عشر من نوفمبر عام 2023، في معهد لانجون لزراعة الأعضاء بجامعة نيويورك. وفيها، أُخذت الكُلية والغدة الصعترية من خنزير، وفرته شركة «ريفيفيكور» Revivicor، وهي شركة تابعة لشركة التقنيات الحيوية «يونايتد ثيرابيوتكس» United Therapeutics، ومقرها ولاية فيرجينا الأمريكية. أُدخل على الخنزير تعديل جيني واحد، أدى إلى تعطيل جين GGTA1، بهدف وقف إنتاج مادة سكرية باسم «ألفا-جال» Alpha-gal على أسطح الخلايا. إذ تبين أن هذه المادة تسبب رفض الجسم للعضو الذي توجد به عند استزراعه في الرئيسيات غير البشرية.
وعلى أثر هذا التعطيل الجيني، بعد الجراحة مباشرة، بدا أن الكُلية بحال جيدة وتنتج البول. غير أنه بعد 33 يومًا من الجراحة، تدهورت فجأة وظائف الكلية، وأظهرت خزعة أنها تتعرض للرفض من الجسم وللإتلاف بفعل أجسام مضادة. وهنا، أبدل الفريق الجراحي بلازما دم المريض بأخرى جديدة وأعطاه ستيرويدات وعقار باسم «بيجاسيتاكوبلان» Pegcetacoplan، ما أدى إلى وقف عملية وسم الجهاز المناعي لخلايا الكلية من أجل استهدافها وتدميرها. غير أنه في اليوم التاسع والأربعين، أظهرت خزعة أخرى حدوث رفض من نوع مختلف للكُلية، تسللت فيه خلايا تائية من الجسم إلى سطح الكلية. وعولج هذا الرفض بإعطاء علاج كابت للمناعة لمتلقي الكُلية، أدى إلى استنزاف الخلايا التائية لديه وحال دون رفض جسمه للكلية. كذلك استعادت الكُلية وظائفها بالكامل. واختار الفريق البحثي إنهاء التجربة بعد 61 يومًا من بدايتها.
نتائج فحوص الجهاز المناعي
بعد الجراحة، حلل الفريق البحثي دم متلقي الكُلية للوقوف على شكل استجابة الجهاز المناعي لها على المستوى الجزيئي. وهنا، برهن الفريق البحثي على أن التعبير عن الجينات المرتبطة بالرفض المناعي للأعضاء المستزرعة - مثل الجينات CXCL9، وCXCL10، وCXCL11 - تزايد تدريجيًا في الكلية المستزرعة، لكنه انخفض فور التصدي العلاجي لهذا الرفض. وفي اليوم الثالث والثلاثين بعد الجراحة، رُصدت مستويات مرتفعة من الخلايا البلعمية الكبيرة، والخلايا القاتلة الطبيعية، اللتان تلعبان دورًا في الجهاز المناعي الفطري، كما لوحظ ارتفاع في عدد الخلايا التائية التي تستعد لمهاجمة الكُلية. ويرى محيي الدين أن هذا يومئ إلى أن الخلايا التائية تلعب دورًا أكبر مما اعتُقد سابقًا في عملية رفض الجسم للأعضاء المستزرعة. وأضاف أن تحليل دم متلقي الكُلية المُستزرعة قد يساعد الأطباء الإكلينيكيين في رصد حدوث الرفض وعلاجه.
أما مونتجومري، فيرى أن هذه الجراحة قد تدلنا أيضًا على ماهية التعديلات الجينية الواجب إدخالها على الخنازير المأخوذة منها الأعضاء. فمع أن أغلب الأعضاء المأخوذة من الخنازير تكون قد خضعت لعشرة تعديلات جينية على الأقل للحد من احتمالية رفض جسم المتلقي لها، في الجراحة المذكورة، حسبما يوضح مونتجومري، كان حذف الجين GGTA1 وحده كافيًا لمنع رفض الجسم للعضو المستزرع فورًا. ودلالة ذلك أنه يمكن للعلماء تربية خنازير تحمل هذه الطفرة الجينية، في حين أن الخنازير التي أدخلت عليها عدة تعديلات جينية ستحتاج إلى استنساخها.
على أن مونتجومري وفريقه البحثي يقرون بضرورة التحقق من فاعلية استخدام أعضاء الخنازير التي خضعت للحد الأدنى من التعديلات الجينية في التجارب على المتوفين دماغيًا والأحياء. وفي الوقت الحالي، يجري مع فريقه تجارب إكلينيكية بالتعاوُن مع شركة «يونايتد ثيرابيوتكس». ويشار إلى أنهم كانوا قد استزرعوا آنفًا كُلية خضعت للتعديل الجيني نفسه في شخص حي، إلا أنها فشلت في أداء وظائفها قبل مرور شهرين على استزراعها بسبب مرض فشل القلب الذي كان متلقي الكلية آنذاك يعاني منه بالفعل.
هذه ترجمة المقال الإنجليزي المنشور في دورية Nature بتاريخ 13 نوفمبر عام 2025.
doi:10.1038/nmiddleeast.2025.198
تواصل معنا: